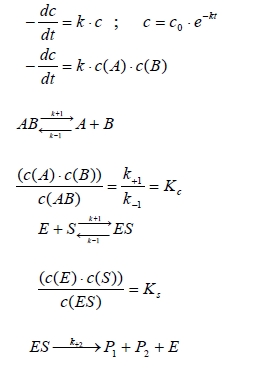Autor: prof. dr Midhat Jašić
Kontakt: midhat.jasic@untz.ba
Pigmenti su prirodne tvari, nosioci boje, a nalaze se u stanicama i tkivima biljaka. Voće i povrće su posebno privlačni zbog svoje jasne, atraktivne boje koja potječe od pigmenata. Žute i narančaste boje potječu od karotenoida. Crvene, plave i ljubičaste boje potječu od flavonoidnih spojeva. Zelena boja lista potječe od klorofila koji je zaslužan za fotosintezu, za disanje. Kod mnogih vrsta voća i povrća pomoću boje se određuje njihov kvaliteta i trajnost. Obojenje može biti rezultat prisustva pigmenata u tkivima ili optičkih efekata zraka svijetlosti. Prirodni pigmenti su vrlo podložni hemijskim promjenama, a naročito pri zrenju voća. Osjetljivi su na hemijske i fizikalne utjecaje tokom prerade. U prehrani značajna mjesta zauzimaju pigmenti, jer mnoge medicinske studije ukazuju na njihov antioksidtivni karakter. Boja se mjeri pomoću različitih kolorimetara. Takvi uređaji mjere karakteristiku svjetla odbijenog od površine materijala kojem se mjeri boja.
Biljni pigmenti – boje boje u voću i povrću
Boja je značajno organoleptičko svojstvo većine voćnih i povrtnih plodova kao i proizvoda koji se od njih dobijaju. Boja voća i povrća je rezultat zajedničke percepcije više pigmenata bilo odvojeno bilo u komleksu. Tradicionalno se crvena, žuta i plava boja smtraju primarnim bojama. Na osnovu boje mogu se odrediti slijedeće karakteristike: zrelost, stupanj rafinacije, čistoća, svježina kao i ispravnost proizvoda. Boja i izgled često pružaju informacije o identitetu proizvoda, kvaliteti i aromi. Preko boje možemo biti upozoreni na mikrobiološko kvarenje proizvoda. Boja može nastati i djelovanje topline na šećere, odnosno karamelizacijom (boja tosta, smeđa boja karamela, itd.). Tamna boja može biti i posljedica hemijskih interakcija između šećera i proteina odnosno reakcija posmeđivanja ili Maillard-ovih reakcija. Do kompleksnih promjena boje dolazi i kada organske komponente hrane dolaze u kontakt s zrakom, te prilikom kuhanja. Krajnja boja je posljedica kombinacije različitih faktora.Najčešće boje voća i povrća su: zelena,crvena,žuta i narandžasta, plava i purourna i bijela. Zeleno voće i povrće između ostalog sadrži antioksidanse, kao što su lutein i indoli.
Zeleno voće i povrće je na primjer: avokado, zelene jabuke, zeleno grožđe, kivi, limete, zelene kruške, grah u mahunama, kupus, celer, krastavci, zelena salata, poriluk, brokula, grašak, zelena paprika, špinat, tikvice, kineski kupus, kelj, artičoke, šparoge i jestive zelene klice. Plodovi, klice i listovi zelenih boja riznica su vitamina i minerala koji pomažu: očuvati dobar vid, smanjiti rizik od nastanka nekih vrsta raka, jačati kosti i zube.
Tabela 15. Pregled pigmenata koji daju boju voću i povrću
| PIGMENTI | FLAVONOIDI | KAROTENOIDI | DRUGI SPOJEVI |
| Plavi i Purpurni | Antocijanidini Flavonoli, Flavan-3-oli, Proantocijanidini | Elaginska kiselina Resveratrol | |
| Zeleni | Flavoni,Flavanoni Flavonoli | Beta-karoten Lutein Zeaksantin | Indoli, Isotiocianati Organosulfurni spojevi Hlorofil |
| Bijeli | Flavonoli i Flavanoni | ||
| Žuti i narandžasti | Flavonoli i Flavanoni | Alfa-karoten Beta-karoten Betakriptoksantin Zeaksantin | Indoli, Isotiocianati Organosulfurni spojevi |
| Crveni | Antocijanidini Flavonoli, Flavoni Flavan-3-oli Flavanoni Proantocijanidini | Likopen | Elaginska kiselina Resveratrol |
Među sastojcima plodova kod kojih prevladava bijela boja jest i alicin, koji sadrže češnjak i bijeli luk. Bijela boja prevladava u proizvodima kao što su : banane, bijele nektarine, bijele breskve, bijele kruške, smeđe kruške, datulje, ingver, gljive, bijeli luk, korijen peršina, bijeli krumpir, češnjak, repa i cvjetača. Voće i povrće bijele boje štite srce i krvne žile jer smanjuju razinu kolesterola u krvi i smanjuju rizik od nastanka nekih vrsta raka. Narandžasti i žuti plodovi sadrže više vrsta antioksidansa, kao što su vitamin C, karotenoidi i bioflavonoidi, a to su : žute jabuke, marelice, dinje, grejpfrut, limune, mango, nektarine, naranče, breskve, mandarine, ananas, žute kruške, kukuruz, korabu, žuti paradjz, mrkvu, žuti krumpir i tikve. Svakodnevno konzumiranje žutog ili narančastog voća i povrća pripomoći će pri: smanjenju rizika od nastanka nekih vrsta raka,zaštiti srca,očuvanju dobrog vida, jačanju imunološkog sistema. Povoljnim učincima voća i povrća crvene boje na zdravlje doprinose i pigmenti, kao što su na primjer antocijanin i likopen, koji su antioksidansi. Plodovi crvene boje: crvene jabuke, crvene naranče, trešnje, crveno grožđe, crvene i ružičaste grejpfrute, šipak, maline, jagode, paradjz, lubenice, crveni kupus, rotkvice, crveni krumpir, rabarbara i radić. Crvena boja voća i povrća štiti srce,čuvati pamćenje,smanjivati rizik od više vrsta raka,štititi mokraćne organe.
Tabela 16. Neki primjeri pigmenata i pripadajućih vrsta voća i povrća
| BOJA | PIGMENT | VOĆE I POVEĆE |
| CRVENA | Antocianini | Jagoda,kupina,višnja,jabuka |
| Likopen | Paradajz lubenica | |
| Betacianini | Repa | |
| NARANDŽASTA | Beta-karotene | Mrkva,mango,kaisija, Bundeva |
| Beta-kriptoksantin | Narandže I tangerine | |
| PLAVA/PURPURNA | Antocianini | Šljive patlidžani , |
| ŽUTA | Lutein, Zeaksantin | Kukuruz , avokado |
| Kurkumin | Tumeric (cari) | |
| ZELENA | Klorofil | Brokule,spana, kupus, zeleni čaj |
| CRNA | Thearubigens | Crni čaj |
| Antocianini | Kupine |
Mnogi su pigmenti nestabilni tokom prerade i skladištenja. Prevencija nepoželjnih promjena je vrlo teška, a u nekim slučajevima i nemoguća. Na stabilnost pigmenata utječu mnogi faktori kao što su: svijetlost, kisik, teški metali, oksidansi, reducensi, temperatura, aktivitet vode, pH.
Jedna od najraširenijih grupa pigmenata spada u grupu porfirina. Porfirini se nalaze u obliku klorofila u zelenim biljkama. Općenito, pigmenti se mogu svrstati u dvije grupe: pigmenti biljnog porijekla i pigmenti životinjskog porijekla, a i jedni i drugi mogu biti: topivi u uljima (klorofili, karotenoidi) i topivi u vodi i staničnom soku
Klorofili i karotenoidi
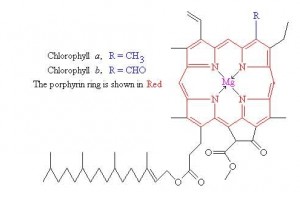
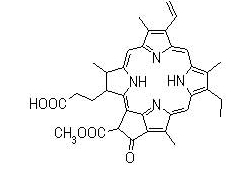
Klorofil. Klorofil je pigment zelenih biljaka, algi i fotosintetskih bakterija, koji je topiv u uljima. Predstavlja kompleks magnezija deriviran iz porfirina. Porfirin je nezasićena makrociklička struktura koja sadrži četiri pirolna prstena vezana preko ugljika. Klorofil se nalazi u lamelama intracelularnih organela zelenih biljaka tj. u kloroplastima. Odgovoran je za fotosintezu i time ima važnu ulogu u održavanju života na Zemlji. Fotosinteza se praktički odvija nakon primanja svjetlosti u kloroplastu, pri čemu se svjetlosna energija konvertira u hemijsku putem ATP i NADPH. Ovaj proces je osnova za sintezu organskih molekula iz CO2 . Primarna ulogu hlprofila je proizvodnja ugljikohidrata iz ugljik (IV) oksida i vode fotosintezom, što se na kraju može sumarno prikazati jednadžbom nastanka života :
CO2 + H2 O + svjetlost —> C6H12O6 + O2
H2O + svjetlost + ADP + P —> O2 + ATP + ee- + NADP+ + H —> NADPH
CO2 + ATP + NADPH —> C6H12O6
Fotosinteza se odvija kod autotrofnih organizama i sastoji se od dva ključna koraka :
• uklanjanje hidrogen (H) atoma iz molekule vode
• redukcija karbon dioksida (CO2) pomoću hidrogen atoma u cilju formiranja organske molekule
Redukcija carbon dioxida (CO2) pomoću hidrogen atoma poznata je kao Calvin Ciklus .
6CO2 + 12H2O -> C6H12O6 + 6H2O + 6O2
Svjetlost snabdijeva kloroplast energijom u formi fotona u cilju :
• transfera elektrona iz vode do nikotinamid adenin dinucleotid fosfata (NADP+) formirajući NADPH i
• generiranja Adenozin Trifsofat ( ATP) – nukleotid sa tri fosvat grupom .
Promjena ATP –a u ADP stavra raspoloživu energiju neophodnu za procese u stanici. Pri tome se ADP-u stvaraju mogućnosti da prihvati drugu fosfatnu grupu i ponovo se sintetiše ATP. Elektroni (e−) I protoni (H+) odvajaju vodikov atom od molekule vode.
2H2O -> 4e− + 4H+ + O2
Pri tome elektroni obavljaju dvije funkcije :
- reduciraju NADP+ do NADPH ( Calvin ciklus ) i
- postavljaju elektorhemijsko punjenje tako što pumpaju protone iz stroma kloroplasta u unutarnjost tilakoida ( granule membrane koje sadrže fotosintetiski pigmet, npr hloropfil u kojima je reakcija ovisna o svjetlosti)
Klorofil je vezan je za karotenoide, lipide i lipoproteine. Između tih molekula postoje slabe nekovalentne veze, koje se vrlo lako mogu prekinuti. Tokom fotosinteze u stanicama klorofil je zaštićen od svjetla jer ga okružuju karotenoidi i lipidi. Kada klorofil izgubi tu zaštitu zbog starenja biljke, ekstrakcije pigmenta iz tkiva ili zbog oštećenja stanice tokom procesiranja, on se pod utjecajem svjetlosti degradira pri čemu nastaju slijedeći produkti fotodegradacije:
- metil etil melemid,
- glicerol,
- mliječna, limunska, sukcinska i malonska kiselinu te
- alanin
U prirodi je pronađeno nekoliko tipova klorofila koji se mođusobno razlikuju po strukturi kao što su klorofil a, b, c d, bakterioklorofil i klorofil klorid. Klorofil a i b se u zelenim biljkama nalaze u omjeru 3:1. Klorofil a sadrži metil grupu i plavo-zelene je boje, a klorofil b formil grupu i žuto-zelene je boje. U algama postoje i klorofil c i d. Bakterioklorofil i klorofil klorid se nalaze u fotosintetskim bakterijama i zelenim sulfatnim bakterijama. Skladištenje određenog povrća (luk, mrkva, bijeli krompir) može dovesti do biosinteze klorofila. U ovom slučaju zelena boja je nepoželjna. Nakupljanje klorofila u bijelom krompiru izaziva biosintezu gorkog i toksičnog aklkaloida solanina. Klorofil je važan kao indikator svježine i zrenja voća i povrća.Degradacija kvaliteta zelenog povrća je gotovo uvijek povezana pojavom žute boje ili gubitkom akumuliranog klorofila. U većini slučajeva nestanak klorofila je uzrokovan smanjenjem njegove sinteze i povećanjem biorazgradnje. Skoro svaki tip prerade ili skladištenja uzrokuje destrukciju pigmenta klorofila. Ove reakcije se ubrzavaju zagrijavanjem i katalizira djelovanjem kisele sredine. Do promjene boje klorofila dolazi kada se Mg – ioni iz porfirinske jezgre iskristališu ionom kiseline pri čemu nastaje feofitin
Promjene u molekuli klorofila koje mogu izazvati gubitak boje su:gubitak magnezija, uklanjanje formil i metil grupe te oksidacija prstena. Klorofilaza je enzim koji može katalizirati degradaciju klorofila. To je esteraza koja cijepa fitol iz klorofila, te nastaju: klorofilid i feoforbid. Gubitak zelene boje tokom termičke obrade, rezultat je nastajanja :feofitina i pirofeofitina.Blanširanje i sterilizacija mogu reducirati sadržaj klorofila. Derivati klorofila koji nastaju tokom termičke obrade mogu se podijeliti u dvije grupe ovisno da li sadrže magnezij ili ne. Derivati koji sadrže magnezij su zeleni, dok oni koji ne sadrže su maslinasto-smeđi. Derivati koji ne sadrže magnezij mogu u prisustvu iona cinka i bakra tvoriti kompleks koji je zelene boje. Prva promjena koja se dešava na molekuli klorofila tokom zagrijavanja je izomerizacija. Atomi magnezija se vrlo lako zamjene u molekuli klorofila s atomima vodika te se dobije feofitin, maslinasto-smeđe boje. U vodenim otopinama reakcija je ireverzibilna. Klorofil je osjetljiv na prisustvo kiselina jer dolazi do njegove degradacije. U biljci se pigmenti i kiseline nalaze u istoj stanici ali odvojeno. Međutim, kuhanjem se povećava permeabilnost membrana te kiseline i pigmenti dolaze u direktan kontakt. Kada se zeleno povrće stavi u kipuću vodu uočava se pojačanje boje, što se može objasniti izlaženjem plina iz intracelularnog prostora, koji u svježem povrću reflektira svjetlo i ublažava boju. Brzina i jačina promjene ovise o nekoliko faktora.
Tako, npr. klorofil a se brže gubi od klorofila b, a također se konvertira u feofitin 7-9 puta brže nego klorofil b. U kiselom mediju se gubi više klorofila. Kuhanje zelenog povrća u velikoj količini ključale vode kako bi se razrijedila kiselina i s poklopcem otvorenim kako bi se eliminirale hlapive kiseline jesu praktične tehnike minimaliziranja utjecaja kiselina na boju. Ako se povrće kuha u alkalnoj vodi dolazi do saponifikacije formilne i metilne esterske grupe. Nastala sol se naziva klorofilin. Povrće kuhano u takvoj vodi nema dobru strukturu jer se razgradi hemiceluloza. Klorofil b je s obzirom na temperaturu stabilniji od klorofila a. Promjena klorofila tokom termičkog tretiranja ima slijed:
klorofil → feofitin → pirofeofitin
Degradacija klorofila u termički obrađenom povrću ovisi o pH tkiva povrća. U alkalnom mediju klorofil je stabilan za razliku od kiselog medija. Prilikom zagrijavanja može doći do smanjenja pH za 1 jedinicu zbog oslobađanja kiselina iz tkiva. Derivati klorofila odgovorni su za maslinato-smeđu boju konzerviranog povrća. Vodikovi atomi u derivatima klorofila se vrlo lako zamjene s ionima cinka ili bakra i tvore komplekse zelene boje. Ti kompleksi su stabilniji u kiselom mediju nego u alkalnom. Metalni kompleksi se tvore i unutar biljnog tkiva, te je utvrđeno da se kompleksi a tvore brže od kompleksa b.
Klorofil se oksidira kada se otapa u alkoholu ili drugim otapalima, te kada je izložen zraku. Taj proces se naziva alomerizacija. Na taj način dobije se proizvod plavo-zelene boje.Kako bi se sačuvala zelena boja konzerviranog povrća potrebno je:zadržati klorofil, formirati ili zadržati njegove zelene derivate (klorofilide) ili omogućiti nastajanje metalnih kompleksa koji su zelene boje. Dodatak alkalnog agensa konzerviranom zelenom povrću može poboljšati zadržavanje klorofila tokom prerade. U tu svrhu vodi se dodaju kalcij oksid i natrij dihidrogen fosfat kako bi se pH proizvoda zadržao ili povećao do pH 7. Grašak, mahunarke, špinat i drugo zeleno povrće gubi jasno zelenu boju.
Blanširanjem na nižim temperaturama od temperature potrebne za inaktivaciju enzima postiže se bolje zadržavanje boje jer se smatra da su klorofilidi termički stabilniji. Temperature bi trebale biti između 54 i 76 °C.
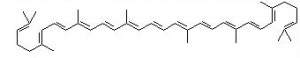
Karotenoidi. Pigmenti grupe karotenoida su topivi u uljima i organskim otapalima, a boja im varira od žute preko narančaste do crvene što podrazumijeva da se nalaze u narančastom, žutom, crvenom i zelenom voću i povrću. Često se nalaze zajedno sa klorofilom u kloroplastima, ali se nalaze i u drugim kromoplastima te slobodno u kapljicama masti. Većina voća i povrća sadrži kompleksne smjese karotenoida. Karotenoidi se nalaze u žutom voću i povrću i u kloroplastima zelenog lišća, gdje su maskirani klorofilom a kako biljka stari oni dolaze sve više do izražaja. Sadržaj karotenoida se tokom zrenja voća povećava. Općenito vrijedi da se najveće koncentracija karotenoida nalazi u tkivima s najvećim sadržajem klorofila. Biosinteza karotenoida nakon branja voća i povrća ovisi o temperaturi skladištenja, svjetlosti, kisiku i zrelosti tkiva prije samog branja. Karotenoidi uključuju:
- narančaste karotene (mrkva, kukuruz, marelica, breskva, agrumi, bundeva),
- crveni likopen (paradjz, lubenica, marelica),
- žuto-narančasti ksantofil (kukuruz, breskva, paprika, bundeva),
- žuto-narančasti krocetin (šafran).
Razlikujemo dvije strukturne grupe karotenoida:
• karoteni i
• ksantofili.
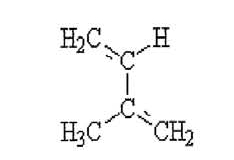
Osnovnu strukturu karotenoida čine kovalentno povezane izoprenske jedinice.Danas poznajemo oko 600 karotenoida, a u voću i povrću ih ima oko pedesetak. Najpoznatiji karotenoidi su beta karoten, likopen i lutein.
To su lančani polinezasićeni spojevi čija je osnovna jedinica izopren.. Na kraju svakog lanca nalazi se ili prsten ili otvoreni lanac i po tome se karotenoidi međusobno razlikuju. Boja ovisi o oscilaciji elektrona duž lanca. Konjugirane dvostruke veze karotenoida nalaze se u trans obliku. Cis izomeri nekoliko karotenoida postoje u biljnom tkivu, posebno u algama. Reakcije izomerizacije započinju djelovanjem topline, izlaganjem organskom otapalu, djelovanjem kiseline i iluminacijom otopine (posebno ako je prisutan jod). Najzastupljeniji karotenoid u biljnom svijetu je β-karoten. Neki karotenoidi pronađeni u biljkama:
- α-karoten (mrkva),
- kapsantin (crvene papričice, paprika),
- zeaksantin.
Mnogi faktori utječu na sadržaj karotenoida u biljkama. U nekom voću zrenje može uzrokovati velike promjene karotenoida. Npr. u paradjzu se sadržaj karotenoida, a posebno likopena značajno povećava tokom zrenja, s tim da koncentracija varira ovisno o stadiju zrelosti. Čak i nakon branja u paradjzu se karotenoidi sintetiziraju. S obzirom da svjetlost stimulira biosintezu karotenoida, izlaganjem voća i povrća svjetlosti dolazi do promjene njihove koncentracije. Ostali faktori koji utječu na koncentraciju karotenoida su: klimatski uvjeti uzgoja, upotreba pesticida i gnojiva, vrsta tla. Neki karotenoidi su vezani za proteine. U strukturu karotenoida mogu biti uključeni i glikozidi npr. krocein u šafranu. Vrlo je bitna veza karotenoida s vitaminom A. Molekula β-karotena se u tijelu konvertira u dvije molekule vitamina A koji je bezbojan. β-karoten u svojoj strukturi ima dva β-ionska prstena, pa je najaktivniji. Drugi karotenoidi, kao što su α-karoten, γ-karoten i kriptoksantin, su također prekursori vitamina A, ali zbog malih razlika u hemijskoj strukturi nastaje samo jedna molekula vitamina A. Karotenoidi imaju važnu ulogu u fotosintezi i čuvanju svjetla u biljnim tkivima. U svim tkivima gdje se nalazi klorofil karotenoidi skupljaju svjetlosnu energiju. Njihova fotoprotektivna uloga proizlazi iz njihove mogućnosti da “zarobe” i inaktiviraju reaktivni kisik koji se stvara kada je biljka izložena svjetlu i zraku. Specifični karotenoidi prisutni u korijenju i lišću služe kao prekursori absicinske kiseline (tvar koja je hemijski glasnik i regulator rasta)
Oni su stabilni s obzirom na toplinu, ali do gubitka boje dolazi zbog oksidacije. Karotenoidi se mogu lako izomerizirati pod djelovnjem topline, svjetla ili kiseline. Glavni uzrok degradacije karotenoida je oksidacija. Mehanizam oksidacije u prerađenoj hrani je kompleksan i ovisi o mnogim faktorima. Pigment se može degradirati autooksidacijom sa atmosferskim kisikom brzinom koja zavisi od inteziteta svjetlosti, toplinskog tretmana. Karotenoidi se lako oksidiraju zbog velikog broja konjugiranih dvostrukih veza. Takve reakcije izazivaju gubitak boje karotenoida u hrani i to je najvažniji mehanizam njihove degradacije. Stabilnost određenog pigmenta na oksidaciju uveliko ovisi o okolini. Unutar tkiva pigmenti su zaštićeni od oksidacije. Fizičko oštećenje tkiva ili ekstrakcija karotenoida povećava njihovu osjetljivost na oksidaciju. Čuvanje karotenoida u organskom otapalu će ubrzati razgradnju. Zbog konjugiranih i nezasićenih veza produkti degradacije su vrlo kompleksni. Tokom oksidacije najprije se formiraju epoksidi i karbonili. Daljnjom oksidacijom nastaju kratkolančane mono- i dioksigenirane komponente koje uključuju i epoksi-β-ion. Epoksidi se uglavnom tvore iz krajnjih prstena što rezultira gubitkom provitaminske aktivnosti. Oksidativna razgradnja β-karotena je pojačana u prisutnosti sulfita i metalnih iona. Karotenoidi su relativno stabilni tokom skladištenja i rukovanja voćem i povrćem. Zamrzavanje uzrokuje male promjene u sadržaju karotenoida, dok blanširanje ima znatan utjecaj i uzrokuje povećanje. Razlog tome je inaktivacija lipogenaze koja katalizira oksidaciju karotenoida. Tokom sterilizacije dolazi do cis/trans izomerizacije. Kada se primjenjuje ekstruzija ili zagrijavanje na visokoj temperaturi u ulju karotenoidi se izomeriziraju ali i termički degradiraju. Na visokoj temperaturi dolazi do stvaranja hlapivih komponenti. Karotenoidi su podložni trans-cis izomeriji kada su izloženi svjetlu ili toplini, a posebno u prisustvu kiselina. Kuhanje mrkve 30 min dovodi do povećanja koncentracije cis izomera β- karotena.
U proizvodnji hrane karotenoidi su prilično otporni na toplinu, promjenu pH, te na tretiranje vodom, ali su vrlo osjetljivi na oksidaciju kada dolazi do promjene boje i uništenja vitamina A Karotenoidi se mogu tokom proizvodnje hrane mijenjati zbog autooksidacije i izomerizacije u prisustvu organskih kiselina. Dehidrirano povrće kao što je mrkva, kada se izloži zraku gubi boju zbog oksidacije nezasićenih molekula. Ova pojava se odnosi i na mrkvu sušenu smrzavanjem i toplinom, ali se ovaj efekat može smanjiti ako se povrće blanšira prije sušenja. Neblanširana sušena mrkva skladištena 6 mjeseci sadrža 9 mg karotena po 100 g suhe tvari, dok blanširana sadrži 54 mg. To je zato jer se tokom blanširanja kidaju lipoproteinski kompleksi i karotenoidi se otapaju u oslobođenim lipidima. Konzumacija voća i povrća koje sadrži veliku količinu karotenoida je povezana sa smanjenjem pojave raka kod ljudi. U posljednje vrijeme više se prate cis-izomeri i njihovo fiziološko značenje.
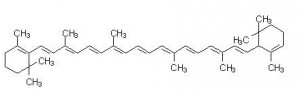
Beta karoten. Najčešći karotenoid, koji je međuprodukt u sintezi vitamina A (retinola), a može se izolirati iz mrkve (prvi put izoliran 1831). Uz ß-karoten u malim količinama uvijek se nalaze Lkaroten, G-karoten i D-karoten. Beta karoten je široko rasprostranjeni biljni pigment koji se nalazi u voću i povrću u svim nijansama od žute i narandžaste pa sve do tamno-zelene boje (mrkva, dinja, kruška, jabuka, špinat, breskva, marelica, mango, bundeva, itd.) Organizam ga prema svojim potrebama pretvara u vitamin A, a prednost nad vitaminom A je u tome što nema štetnog djelovanja niti kada se uzima u većim količinama.
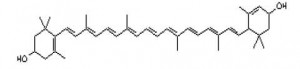
Beta karoten je jaki antioksidans, jača odbrambeni sistem, igra važnu ulogu u sprječavanju nastanka raka, smanjuje rizik od arteroskleroze, srčanog i moždanog udara, te štiti od stvaranja mrene. Štiti kožu od opasnog spektra UV zračenja pa se osim u kremama za sunčanje preporučuje i interno nekoliko sedmica prije izlaganja suncu. Lutein. C40H56O2, nalazi se u zelenom i žutom lišću. Lutein je hidroksi–derivat ß-karotena. Prehrana sa mnogo luteina (zeleno lisnato povrće, špinat, brokula), povoljno djeluje na krvožilni sistem i štiti od malignih oboljenja, te štiti očnu leću od mrene.
Kriptoksantin. C40H56O, je monohidroksi–derivat ß-karotena. Nađen je slobodan i esterificiran u mahunama i paprici, a glavni je pigment mandarine. Kriptoksantin ima polovicu aktivnosti vitamina A.
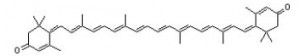
Rodoksantin. C40H50O2, primjer je ketonskih karotenoida. Budući da su sve dvostruke veze konjugirane uključujući i veze karboksilnih grupa, njegove apsorpcijske vrpce leže dalje, nego vrpce bilo kojeg drugog karotenoida.
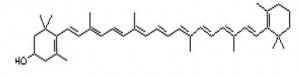
Likopen. Biljni pigment koji voću i povrću daje crvenu boju. Najvažniji izvor likopena je paradajz. S obzirom da je likopen lipofilno jedinjenje, veći procenat likopena nalazi se u termički prerađenom paradajzu sa uljem (kečap, paradajz sos) nego u svježim plodovima. Ostali izvori likopena su lubenica, ružičasti grejpfrut, kajsije i dr.
Iako je likopen dugo bio zapostavljan u istraživanjima zbog nedostatka provitaminske aktivnosti, odnosno zato što se u organizmu ne konvertuje u vitamin A, danas se u stručnoj javnosti smatra za jedan od najinteresantnijih karotenoida. Brojne naučne studije pokazale su veliku antioksidativnu sposobnost likopena, daleko veću u odnosu na druge karotenoide. Još nije precizno uspostavljen preporučen dnevni unos likopena, ali mnoge studije upućuju na najmanje 3-6 mg dnevno da bi se postigli optimalni efekti.
Tabela 17. Sadržaj likopena u voću, povrću i prerađevin
| Voće, povrće i prerađevine | Sadržaj likopena (mg / 100) g) |
| Kajsija | 0,005 |
| Kajsija (kompot) | 0,065 |
| Ružičasti grejpfrut | 3,36 |
| Lubenica | 4,10 |
| Papaja | 2 – 5,30 |
| Paradajz (svjež) | 0,90 – 4,20 |
| Kuvani paradajz | 3,70 |
| Paradajz sos | 12,71 |
Zbog svog lipofilnog karaktera likopen ima tendenciju taloženja u tkivima, i to prije svega u prostati, jetri, nadbubrežnoj žlijezdi. Upravo povećanje nivoa likopena u tkivima smanjuje oksidativna oštećenja bioloških sistema, što uključuje oštećenja ćelijskih membrana i drugih struktura, kao što su DNK molekuli, lipidi, proteini.Do joštećenja ovih struktura i molekula dolazi usljed dejstva slobodnih radikala.
Pigmenti topivi u vodi i staničnom soku
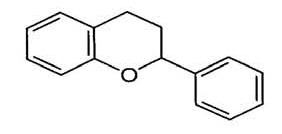
Flavonoidi. Pigmenti topivi u vodi i staničnom soku čine veliku skupinu hemijskih spojeva. Flavonoidi se prije svege nalaze u ljuskama voća (jabuke, trešnje) i povrća (paradajz). Poznato je ukupno oko 4.000 – 5.000 raznih vrsta flavonoida. Plavo-ljubičasto voće i povrće sadrži flavonoide ( antocijanine, fenole i druge spojeve). Voće i povrće plave i ljubičaste boje su naprimjer: borovnice, kupine, crni ribiz, šljive, ljubičaste smokve, ljubičasto grožđe, grožđice, patlidžan, ljubičasti krumpir, ljubičaste šparoge itd. Flavonoidi predstavljaju najveću i najznačajniju skupinu biljnih fenola. Izvode se iz flavana (2-fenol-benzo-dihidro-piran) i mogu se podijeliti u pet skupina: antocijanidini, flavoni, flavonoli, flavanoni, katehini, leukoantocijani i proantocijanidini. Iako većina žute boje u hrani potječe od karotenoida, za neke od tih nijansi zaslužni su neantocijanidni flavonoidi. Također su neki flavonoidi odgovorni za Voće, povrće i prerađevine bijelu boju, a oksidacijski produkti koji sadrže fenolne grupe odgovorni su za smeđu i crnu boju. Termin antoksantin se ponekad koristi za grupu flavonoida koji daju žuto obojenje. Razlika između flavonoida je na C-3. Strukture pronađene u prirodi variraju od flavanola (katehin) do flavonola (3-hidroksiflavoni) i antocijana. Flavonoidi uključuju: flavanone, flavononole i flavan-3,4-diole (proantocijanidin).
Antocijanidini, flavoni i flavonoli dolaze u prirodi u vezanom obliku kao glikozidi. Glikozidi antocijanidina zovu se antocijani i crvene su do plave boje, koja je karakteristika brojnih vrsta voća. Flavon i flavonolglikozidi dolaze u svakoj biljnoj vrsti i imaju slabo žutu boju. Flavoni se razlikuju od flavonola u nedostatku OH skupine na C3 atomu srednjeg prstena.
Tabela 18. Neki flavonoidi
| RB | FLAVONOIDI | PRIPADNICI SKUPINE |
| 1 | FLAVONOLI | Quercetin, Kampferol, Miricetin, Izorhamnetin |
| 2 | FLAVONI | Luteolin, Apigenin |
| 3 | FLAVANONI | Hesperetin, Naringenin, Eriodictiol |
| 4 | FLAVAN-3-OLI | Katehin, Galokatein, Epigalokatehin, Epikatehin, Teaflavin, Tearubigin |
| 5 | ANTOCIJANIDINI | Cijanidin, Delfinidin, Malvidin, Pelargonidin, Peonidin, Petunidin |
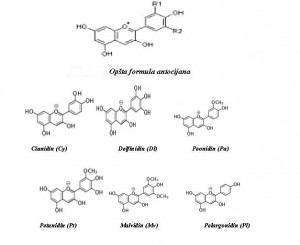
Antocijani. Riječ antocijanin dolazi od dvije grčke riječi, anthos (cvijet) i kyanos (plavo). Antocijani su prisutni u svakodnevnom životu, u voću, povrću, cvijeću. Nalaze se u grožđu, višnjama, jagodama, malinama, rotkvicama, crvenom zelju itd. Danas se antocijani najčešće ekstrahiraju iz grožđa i crvenog zelja, zatim iz bobica bazge, crnog ribizla i crne mrkve. Više od 300 vrsta antocijana je identificirano u prirodi. Iz strukturnih varijacija H, OH i OCH3 grupa na B-prstenu proizilazi 6 različitih aglikona antocijanidina: pelargonidin, cianidin, delfinidin, peonidin, petunidin i malvidin. Osim pelargonidina, grožđe sadrži svih 5 vrsta antocijanidina, sa malvidinom i delfinidinom kao dominantnima. Cianidin je najčešći antocijanidin u prirodi i ekstrakti crvenog zelja, crne mrkve i bobica bazge su u cijelosti na bazi cianidina. Antocijani su rektivne molekule, pogotovo one koje sadrže orto-fenolne grupe (cianidin, petunidin i delfinidin) su više podložne oksidaciji i stvaranju kompleksa sa metalnim jonima. Antocijani uvijek postoje u prirodi kao glikozidi. Aglikoni koji mogu nastati kiselinskom ili enzimskom hidrolizom su izuzetno nestabilni. Glikozidna supstitucija povećava stabilnost i vodotopivost. Supstitucija se pojavljuje na 3. i 5. poziciji A-prstena, rijetko na 7. poziciji. Najčešći glikozidni šećeri su: glukoza, galaktoza, ksiloza, arabinoza i raminoza. Molekule antocijana se mogu međusobno povezivati i acilirati sa aromatskim i alifatskim kiselinama. Te pojave se još nazivaju ko-pigmentacija, što pridodaje njihovoj stabilnosti.
Tabela 19. Šest osnovnih tipova antocijana u voću i povrću
| Antocijani | Voće i povrće u kojima se nalaze |
| Cianidin | Jagode, bazga, crveno zelje |
| Delfinidin | Borovnice |
| Malvidin | Kožica grožđa |
| Pelargonidin | Jagode i rotkvice |
| Peonidin | Brusnice |
| Petunidin | Borovnice |
Antocijani su najzastupljenija grupa pigmenata od svih flavonoida. Najzastupljeniji antocijanini su ekstrahirani iz grožđa (enocijanini). Antocijanini su koncentrirani u kožici grožđa. Na stabilnost antocijana utiću: koncentracija, svijetlo, uticaj aw i molekularni kopigmentacijski efekti. Pigmenti antocijana pokazuju veću stabilnost kada su prisutni u većim koncentracijama. Svjetlost je značajan faktor destabiliziranja. Ispitivanja su pokazala da stabilnost antocijana raste kad se smanjuje aktivnost vode (aw). Kopigmentacija se može pojaviti u biljci, ali i u ekstraktu. Ova grupa ima više od 150 u vodi topivih pigmenata koji su vrlo rašireni u biljnom carstvu. Tako, crvena boja jagoda potječe od dva antocijana: pelargonidin-3-glukozida i cijanidin-3-glukozida.
Antocijanini su vrlo nestabilni. Gubitak boje zamjetljiv je poslije odmrzavanja smrznutog voća i tokom prerade te čuvanja proizvoda od jagoda. Promjena boje posljedica je reakcije antocijana sa nastalim kinonima. Brzina destrukcije antocijana zavisi od pH jer se ubrzava pri višoj pH vrijednosti. Sa aspekta pakiranja postoji mogućnost formiranja kompleksnih spojeva sa metalima kao što Al, Fe, Cu i Sn. Ovi kompleksi općenito rezultiraju promjenom boje pigmenata. Na primjer crvena boja višnje reagira sa kalajem i formira purpurni kompleks. Metal konzervi može biti izvor ovih metala pa je potrebno oblagati ambalažu specijalnim organskim spojevima koji eliminiraju ove neželjene reakcije.
Brzina degradativnih reakcija antocijana slijedi brzinu degradativnih reakcija šećera do furfurala. Koncentracije fruktoze, arabinoze, laktoze i sarboze imaju veći degradativni učinak od glukoze, saharoze i maltoze. Furfural koji nastaje Maillard-ovim reakcijama ili oksidacijom askorbinske kiseline kondenzira s antocijanima i nastaju smeđi produkti. Ova je reakcija ovisna o temperaturi, kisiku, a može se uočiti kod voćnih sokova. Metalni kompleksi antocijana su uobičajeni u biljnom svijetu i oni povećavaju spektar boja. Odavno je otkriveno da premazane metalne limenke čuvaju boju voća i povrća tokom sterilizacije. Istraživanja su pokazala da metalni kompleksi stabiliziraju boju hrane koja sadržava antocijane. Ca, Al, Fe, Sn štite antocijane u soku od brusnice, iako dolazi do negativnog efekta jer se i metali spajaju s taninima koji daju plavo i smeđe obojenje. Djelovanjem SO2 (koncentracija 500-2000 ppm) na voće koje sadrži antocijane kako bi se ono sačuvalo od kvarenja dolazi do gubitka boje koja se može povratiti postupkom desumporiranja (pranjem) prije daljnjeg procesiranja. Antocijani se mogu kondenzirati sami sa sobom ali i sa drugim organskim komponentama. Slabe komplekse tvore sa proteinima, taninima, drugim flavonoidima i polisaharidima. Smatra se da stabilna boja vina potječe od međusobne kondenzacije antocijana. Takvi polimeri su manje osjetljivi na promjenu pH, a i otporni su na obezbojenje pomoću SO2 jer se spajanje vrši na C-4.
Na promjenu boje antocijana mogu utjecati i enzimi. Identificirane su dvije grupe, glukozidaze i polifenol oksidaze. Glukozidaze hidroliziraju glukozidne veze, te nastaje šećer i aglikon. Gubitak boje je rezultat smanjenja topivosti antocijanidina i njihove transformacije u bezbojne produkte. Polifenol oksidaza djeluje u prisustvu o-difenola i kisika i na taj način oksidira antocijane. Enzim najprije oksidira o-difenol u o-benzokinin, koji zatim reagira s antocijanima neenzimskim mehanizmom. Blanširanje voća baš i nema primjenu ali se preporučuje kako bi se inaktivirali enzimi (45-60 sec 90-100 °C). Vrlo niske koncentracije SO2 (30 ppm) inhibiraju enzimsku degradaciju antocijana u višnjama.
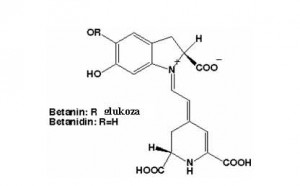
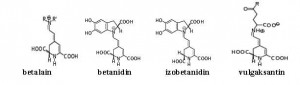
Betalaini. Biljke koje sadrže betalaine slične su boje kao i biljke koje sadrže antocijane. Betalaini su grupa pigmenata u koju se ubrajaju betacijan (crveni) i betaksantin (žuti) na čiju boju ne utječe pH, za razliku od antocijana. Topivi su u vodi i postoje kao soli u vakuolama biljnih stanica. Prisutnost betalaina u biljkama isključuje prisutnost antocijana. Opća formula betalaina predstavlja kondenzirani primarni ili sekundarni amin s betalaminskom kiselinom. Svi betalaini mogu se opisati kao 1, 2, 4, 7,7- pentasupstituirani 1, 7 diazaheptametin sistemi. Betalaine su pigment karakterističan ciklu i najproučavaniji betalaini su betalaini cikle. Različiti betalaini cikle daju razlićitu boju.Najznačajniji betacijani cikle su betanin i izobetanin.
Betaksantin cikle je vulgaksantin, kojem nedostaje aromatski prsten vezan na N-1 i šećer. Ostali pigmenti su :izobetanin, betanidin izobetanidin i vulgaksant betalain betanidin izobetanidin vulgaksantin
Prvi betaksantin izoliran i okarakteriziran je indikaksantin. Pod srednje alkalnim uvjetima betanin se degradira do betalaminske kiseline i ciklodopa-5-O-glukozida. Ova se dva degradacijska produkta također tvore zagrijavanja kisele otopine betanina ili tokom termičkog procesiranja proizvoda koji sadrže ciklu, ali sporije. Dokazano je da askorbinska kiselina štiti crvenu boju, čak i kad je proizvod izložen drastičnim uvjetima npr. sterilizaciji. Prisustvo metala smanjuje stabilnost betalaina. Betalaini su pogodni za upotrebu u prehrambenoj industriji ali pri niskim temperaturama, npr. u mliječnoj industriji za proizvodnju sladoleda i mliječnih napitaka
Na betalaine vrlo rijetko utječe pH prehrambenih proizvoda. Oni su stabilni između pH 4.0 – 7.0, ali ispod i iznad tog pH dolazi do promjene boje. Termostabilnost modelnih sustava ovisi o pH i najveća je u području 4.0 – 5.0. Sok ili kaša cikle imaju veću stabilnost što nam govori da u samoj biljci postoji zaštita. Još jedan od važnih faktora koji utječe na degradaciju betalaina je prisustvo kisika. Kada je kisik odsutan stabilnost pigmenta se povećava.
Oksidacija betalaina se ubrzava u prisustvu svjetla. Prisutnost antioksidansa, kao što je askorbinska i isoaskorbinska kkiselina, poboljšavaju stabilnost.
Bojila kao aditivi u voću i povrću
Bojila – su čiste tvari, koncentrati ekstrakata jestivih sirovina ili sintetskim postupkom proizvedeni hemijski spojevi poznatog sastava, a dodaju se u malim količinama za bojenje namirnica, ne mijenjajući ostala svojstva proizvoda. Bojila mogu biti prirodna i umjetna Bojila pripadaju aditivima , a to su tvari točno poznatog hemijskog sastava, koje se ne konzumiraju kao namirnice, niti su tipičan sastojak namirnice, bez obzira na prehrambenu vrijednost, a dodaju se namirnicama u svrhu poboljšanja tehnoloških i senzorski svojstava.
Bojila se mogu da dodaju namirnicama u tehnološkom postupku proizvodnje, tijekom pripreme, obrade, prerade, oblikovanja pakiranja, transporta i čuvanja. Mješavinom aditiva razumijeva se miješanje dvaju ili više aditiva iste skupine ili različitih skupina, sa ili bez nosača ili razrjeđivača, uz uvjet da je takvo miješanje tehnološki opravdano. Bojila mogu biti na odredjenom nosaču. Nosačima ili razrjeđivačima smatraju se i namirnice. U mješavini aditiva ne smiju se međusobno miješati sljedeći aditivi:
- bojila,
- kalijev i natrijev nitrat,
- natrijev nitrit,
- bifenil,
- ortofenilfenol i natrijev ortofenilfenolat,
- tiabendazol,
- hexametilentetramin,
- borna kiselina i natrijev tetraborat,
- arome,
- trietilcitrat.
Zabranjeno je dodavanje bojila:koncentratu paradjza i proizvodima od paradjza u konzervi ili staklenkama, umacima na bazi paradjza, voćnim sokovima i nektarima te soku od povrća, voću, povrću i gljivama i njihovim prerađevinama u konzervama ili bocama kao i u sušenom obliku, ekstra džemu, marmeladi i želeu te kesten pireu, prženoj kafi, čaju i cikoriji, čajnom ekstraktu i ekstraktu cikorije, pripravcima od čaja, bilja, voća kao pojedinačnoj sirovini ili u smjesi u originalnom ili instant obliku., soli i nadomjescima za sol, začinima i mješavine začina, vinu od grožđa i sličnim fermentiranim proizvodima, voćnim alkoholnim pićima, žestokim voćnim pićima, vinskom octu, hrani za dojenčad i malu djecu (uključujući i hranu za djecu slabog zdravlja), sladu i proizvodima od slada i Ukoliko se sirovinama za izradu navedenih namirnica dopušta upotreba bojila u njihovoj proizvodnji, onda se primjenjuje princip „prijenosa“.
Tabela 20. Bojila
| RB | E broj | Naziv aditiva | Dopuštenost upotrebe |
| 1. | E101 | Riboflavin (I)
Riboflavin-5’-fosfat |
Povrće u ulju, octu i salamuri (izuzev maslina i drugog voća) umaci od povrća (izuzev od paradjza) |
| 2. | E140 | Chlorophylle (I)
Chlorophhylline (II) |
|
| 3. | E141 | Bakreni kompleks
Chlorophylle (I) Chlorophylline (II) |
|
| 4. | E150a
E150b E150c E150d |
Obični, jednostavni Caramel
Caramel-amonijačni Caramel-sulfitno kiseli Caramel-sulfitno/amonijačni |
džem, voćni žele, marmelada i pekmez (izuzev exta đema i extra želea ) i slični voćni namazi, uključujući i niskokalorične proizvode sa ili bez dodatka šećera |
| 5. | E160a
E160c |
Carotenes /smjesa Carotenes(I),
ß-Caroten (II)/Paprica extract, Capsanthin, Capsorubin |
|
| 6. | E162 | Beet red, Betain | kompot od crvenog jagodičastog voća deserti na bazi voća i povrća |
| 7. | E163 | Anthocyanins | kandirano voće i povrće, Mustarda di frutta nektar od povrća citrus baza , voćni sirup (samo citrus sirup) |
| 8. | E100 | Curcumin | sušeni krumpir u granulama ili pahuljicama |
| 9. | E104 | Quinoline Yelow | đem, žele, marmelada i pekmez (izuzev extra đema, marmelade i extra želea) i slični voćni namazi uključujući niskokalorične proizvode sa ili bez dodatka šećera |
| 10. | E110 | Sunset Yellow | |
| 11. | E120 | Carmines, Cochenille,
Carmine acid |
|
| 12. | E124 | Ponceau 4R, CochenilleRed | |
| 13. | E142 | Green S | kandirano voće i povrće, |
| 14. | E160d
E160e E160f |
Lycopin
β-apo-8’-carotenal (C30) β-apo-8’-carotenal C830) ethyleste |
kompot samo crvenog voća |
| 15. | E161 b | Lutein | Pickles, relishes, Chutney i Piccalili |
| 1 | citrus baze | ||
| 1 | voćni sirup (samo citrus sirup) | ||
| 16. | E102 | Tartrazin | Processed mushy i garden peas |
| 17. | E133 | Brillantblue FCF | ( sterilizirani) |
| 18. | E142 | Green S | |
| 19. | E127 | Erythrosine | Biggareaux trešnje u sirupu i koktelima koktel od trešanja i kandirane trešnje |
Zaključak
Boja svježeg voća i povrća potječe od prirodnih pigmenata. Najčešći i najviše zastupljeni prirodni biljni pigmenti, prisutni u svježem voću i povrću su: klorofili, karotenoidi i flavonoidi. Značajni su u formiranju izgleda i ukupnih senzornih svojstava voća, povrća i njihovih preradjevina. Nestabilni su tokom procesa prerade. Boja preradjevina potječe od prirodnih pigmenata ili dodanih bojila. Za vrijeme prerade nastoji se što više očuvati prirodna boja voća i povrća u gotovom proizvodu.Umjetne boje u hrani su najčešće štetne po zdravlje , dok prirodne imaju protektivan karakter. Preveniraju kardiovaskularnih bolesti (bolesti srca, arteroskleroze), rizik od pojave tumora želuca, debelog i tankog crijeva, mjehura, prostate, pluća, dojki, pankreasa, usne šupljine.
Enzimi i enzimsko posmeđivanje u voću i povrću
Razvoj nauke i tehnologija sve brže mijenja svijet oko nas , a naročito znanosti vezane za biotehnologije gdje enzimi zauzimaju sve značajnije mjesto. U prirodi postoji veliki broj enzima koji imaju uticaja na ravnotežu bioloških sistema. Od njihove pojave pa do danas naučnici su ih svrstavali u skladu sa nivoom postignutih saznanja . Danas se najčešće klasificiraju na 6 osnovnih grupa :
– oksidoreduktaze,
– transferaze,
– hidrolaze,
– liaze,
– izomeraze i
– ligaze.
Enzimi su prisutni u biološkim sistemima kao unutarnji ili autohtoni i enzim vanjskog porijekla. U pojmu i shvatanju definicije enzima postoji jedinstvo poimanja da su oni biološki katalizatori tj. ubrzavaju biohemijske procese , a da se sami pri tome ne mijenjaju. Enzimi su bili poznati oduvijek i kako se mijenjao napredak ljudske civilizacije i življenja tako su nalazili svoju primjenu u proizvodnji hrane. Ekspanzija primjene enzima započinje u 20. stoljeću. Moderne nauke biohemija, molekularna biologija su bazirane na jediničnim procesima u kojima enzimi imaju esencijalnu funkciju. Razvoj biotehnologije, pogotovo razvoj genetskog inženjerstva baziran je na primjeni enzimskih preparata. Enzimi u prehrambenoj industriji se koriste u svrhu ubrzavanja biohemijskih procesa, postizanja odredjenih svojstava proizvoda, poboljšavanja ukupne kvalitete proizvoda i sl. Enzimi su po svom sastavu proteini. Hemizam i kinetika djelovanja enzima analogni su teoretskim postavkama kinetike klasičnih hemijskih procesa, pa se i modeli enzimskih procesa baziraju na istim zakonitostima. Razvojem nauka kao što su molekularna biologija i genetsko inženjerstvo rapidno raste i istraživanje enzima i njihovo korištenje u prehrambenoj industriji. U nekim slučajevima enzimi se mogu posmatrati kao aditivi i kao takvi su regulisani odgovarajućim propisima o kvalitetu aditiva. U drugim slučajevima mogu se javiti kao pomoćna sredstva u procesu proizvodnje koji uglavnom još nisu regulisani Fizikalno-hemijska i senzorna svojstva voća i povrća 319 legislativom. Komercijalni enzimi najznačajniju primjenu u industriji prerade voća i povrća imaju kod proizvodnje bistrih sokova gdje spriječavaju pojavu mutnoće i povećavaju stepen iskorištenja polazne sirovine. Zatim kod prerade škroba iz krompira i dobivanja šećera. U oba slučaja dobija se veći prinos iz polaznih sirovina nego kod procesa proizvodnje gdje nisu korišteni enzimi .
Enzimi su se tokom dvadestog stoljeća počeli sve više proizvoditi i koristiti u komercijalne svrhe. U prehrambenoj proizvodnji enzimi nalaze primjenu u preradi mesa i mlijeka, proizvodnji hljeba i peciva, konditorskih proizvoda, ulja i masti kao i preradi i konzerviranju voća i povrća.Najznačajnija primjena enzima u tehnologiji voća i povrća je u proizvodnji bistrih sokova, proizvodnji vina i preradi povrća bogatog škrobom ( krompir ) .Enzimi se takodje koriste i u znanstvene svrhe u oblasti GMO, Novel Food, kao i molekularnoj biologiji , biohemijskom inženjerstvu , biotehnologiji i sl .
Kinetika i hemizam djelovanja enzima
Hemijska priroda enzima.Enzimi ili, kako su se prije zvali, fermenti, biološki su vrlo važna skupina proteina. Oni su katalizatori žive stanice . Cjelokupnost svih biohemijskih pretvorbi je moguća samo zbog prisustva ili ispravnije rečeno, djelovanja enzima . Supstratima nazivamo spojeve koji se hemijski mjenjaju djelovanjem enzima. Koristeći se metodom proteinske hemije, dobiveno je dosad stotine enzima u kristaliziranom stanju, a prvi enzim izoliran u kristalnom obliku bila je ureaza ( Sumner , 1926 ). Za katalitičko djelovanje odgovorno je « aktivno središte ».
Mnogi enzimi pripadaju proteidima, pa se sastoje od proteinskog dijela i od pripadne « prostetske skupine ». Neki enzimi u svojoj aktivnoj formi vežu takvu skupinu reverzibilno, pa protein tada nazivamo apoenzimom ,a prostetsku skupinu koenzimom :
koenzim + apoenzim = ( holo ) enzim
Koenzimi , koji bi se prema sistematici trebali ispravnije nazivati kosupstratima , imaju važnu funkciju pri enzimskom djelovanju.
Enzimi djeluju vrlo specifično. Oni posjeduju specifičnost prema supstratu, tj. oni reagiraju sa tačno određenim međuproduktom metabolizma. Enzimi mogu biti male ili velike molekulske mase, mogu se sastojati od dvije ili više aminokiselina koje su međusobno vezane kovalentnim peptidnim vezama, a molekulska masa im može biti od 10000 do 1000000. Osim aminokiselina mogu na sebe imati vezane i druge spojeve, npr. CHO, fosfate, itd. Enzimi iz supstrata dobijaju sasvim novu komponentu – proizvod:
Enzimi se nalaze u svim živim organizmima i utječu na ukupnu dinamičku biološku ravnotežu. Selektivni su, pa praktički svaki spoj ima svoj odgovarajući enzim koji katalitički djeluje na biohemijske procese tog spoja. Enzimi osim što djeluju selektivno mogu utjecati na smjer reakcije (revrezibilan ili ireverzibilan). Imaju svoj životni ciklus i ne djeluju beskonačno, mada se po osnovnoj postavci regeneriraju. Vremenom se „iscrpljuje“ njihovo djelovanje, tako da im se aktivnost vremenom smanjuje. Životni ciklus, odnosno vrijeme aktivnosti enzima ovisi o:količini supstrata, pH vrijednosti, temperaturi, itd. Pri denaturaciji razara se konformacija enzima. Zbog toga se gubi katalitičko djelovanje iako je sekvencija aminokiselina ostala očuvana .
Klasifikacija i nomenklatura enzima. Međunarodna unija biohemičara i mikrobiologa su objavile šest kompletnih izdanja nomenklature enzima. Još 1950. god. je primjećeno da u nomenklaturi enzimologa postoji odsustvo vodećih autoriteta, iako je već prilično veliki broj enzima bio poznat , a njihova primjena se počela koristiti rapidno . Davanje imena enzima bilo je individualno od strane onih koji su ih otkrili , tako da je jedan enzim imao više različitih imena .
Zbog toga je 1955. god. Generalna skupština međunarodnog udruženja biohemičara uspostavila međunarodnu nomenklaturu za enzime . Ovaj korak je poduzet zajedno sa IUPAC-om . Tako da je do danas uspostavljena kvalitetna nomenklatura kojom se identificiraju enzimi. Enzimi se klasificiraju na osnovu reakcija koje kataliziraju. Koristi se brojni sistem koji je definirala Komisija za enzime. Sastoji se od četiri cifre koje identificiraju enzim. Prva cifra identificira klasu enzima. Druga cifra identificira pod klasu ako enzim nije prisutan u prvoj glavnoj klasi. Primjer djelovanja hidrolaza. Treća cifra identificira pod klasu enzim. Primjer djelovanja glukozidaze.Četvrta cifra identificira specifične enzime i oni su jedinstveni za svaku poznatu enzimsku reakciju . Primjer djelovanja O – glikozidaze. Kod skladištenja i prerade voća i povrća veoma važnu ulogu igraju enzimi klase hidrolaze (lipaze, invertaza, tanaza, klorofilaza, amilaza i celulaza ) i oksidoreduktaze ( peroksidaze, tirozinaze, katalaze, askorbinaze ).
Osnove hemijske kinetike enzima. Kinetika enzimskih reakcija daje kvantitativne odnose između brzine reakcije i koncentracije enzima i supstrata . U hemijskoj se kinetici kao mjera za brzinu reakcije upotrebljva promjena koncentracije u vremenu dc/dt .
Gdje su:
A , B – tvari koje učestvuju u reakciji
c(E) – koncentracija enzima
c(S) – koncentracija supstrata
k – konstanta brzine reakcije
Kc – konstanta ravnoteže
Ks – konstanata supstrata
Km – Michaelisova konstanta
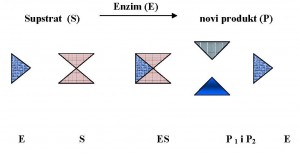
Michaelis-Mentenova teorija. Svaka enzimska reakcija počinje vezanjem supstrata na enzim. Stvarna enzimska reakcija provodi se samo preko kompleksa. Produkti P1 + P2 nastaju u reakciji koja praktički teče do kraja i pri tome se istodobno regenerira katalizator. Michaelis i Menten su predpostavili da ta reakcija određuje brzinu , tj. da je bitno sporija od stvaranja kompleksa enzim-supstrat. Tada je brzina ukupne reakcije koju možemo izravno mjeriti proporcionalna koncentraciji kompleksa enzim-supstrat c ( ES ) , pa možemo brzinu reakcije smatrati mjerom za koncentraciju ES . Ako polazimo od određene količine enzima i postepeno povisujemo koncentraciju supstrata , sve se više enzima prevodi u kompleks ES , brzina reakcije raste dok napokon praktički sav enzim ne predje u ES. Enzim je zasićen , a brzina reakcije poprima maksimalnu vrijednost.Hemijska termodinamika izučava da je konstanta ravnoteže neke hemijske reakcije povezana uz promjenu slobodne energije jednadžbom
ΔG 0 = – RT ln K
Gdje su : ΔG – slobodna energija, R – gasna konstanta, Ttemperatura i K – konstanta ravnoteže.
Reakcije teku sve dotle dok se ne uspostave ravnotežne koncentracije, tj. kada je slobodna energija ΔG = 0. Za samu katalizu bitno je snižavanje energije aktivacije, a ne promjena slobodne energije. To se postiže uzajamnim djelovanjem proteinskog dijela enzima sa supstratom koji se povezuju u kompleks enzimsupstrat. Enzimi ne mogu izazvati hemijsku reakciju niti mogu pomaknuti položaj ravnoteže. Oni snižavaju energiju aktiviranja reakcije (Ea), odnosno omogućavaju većem broju molekula da prijeđu energetsku barijeru (Ea’) čime se reakcija ubrzava. Ukupna energija reakcije (Ereak.) ostaje nepromijenjena. Određeni enzim može sudjelovati i u sintezi i u razgradnji određene tvari.
Metaboliti u stanici se ne nalaze u hemijskoj ravnoteži. Stanje u stanici , kao i u cijelom organizmu , može se opisati kao dinamička ravnoteža. Organizam dobiva energiju putem hemijskih reakcija koje se odvijaju u dinamičkoj ravnoteži . Supstrat se najčešće veže nekovalentno, a može i kovalentno na enzimski protein i tu učvrsti u određeni položaj. Reakcija teče iz tog reaktivnog međuprodukta. Određeni pobočni lanac u aktivnom središtu proteina sudjeluje u katalizi često kao proton- akceptorske , odnosno proton-donorske skupine , u smislu kiselinsko-bazne katalize . Kod reakcija sa dva supstrata , ispravan prostorni raspored molekula supstrata na proteinskom dijelu enzima preduvjet je za katalizu . Takvim se mehanizmom energija aktivacije enzimske reakcije općenito toliko snižava da se brzina reakcije povećavaju i za više od 10 10 puta.
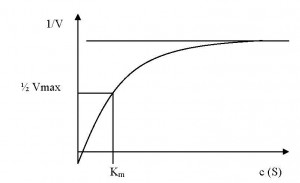
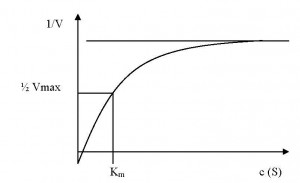
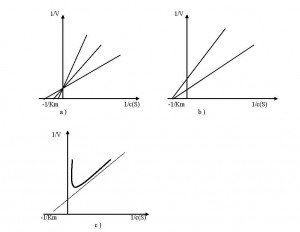
Aktivnost enzima mjeri se brzinom reakcije supstrata . Kinetika enzimskih reakcija pokazuje kako brzina reakcije ovisi samo o koncentraciji enzima i supstrata . Michaelisova konstanta je definirana koncentracijom supstrata kod koje se postiže polovica maksimalne brzine , odnosno kod koje je enzim poluzasićen supstratom. Aktivnost enzima može biti reverzibilno inhibirana . Razni tipovi inhibicije važni su za fiziološku regulaciju enzimske aktivnosti , a od njih možemo spomenuti konkurentnu inhibiciju i alosteričku inhibiciju .Reverzibilna inhibicija enzima ima važnu ulogu u regulaciji metabolizma . Kod konkurentne inhibicije ( slika a ) ostaje odsječak na ordinati 1/Vmax nepromijenjen , ali se povećava nagib pravca ;kod nekonkurentne inhibicije ( slika b ) ostaje odsječak na apcisi –1/ Km konstantan , a povećava se nagib pravca i 1/Vmax . Inhibicija supstratom ( slika c ) dovodi do odstupanja od pravca na Lineweaver – Burkovu dijagramu
a – konkurentna inhibicija , b – nekonkurentna inhibicija , c – inhibicija supstratom . Kod a i b najdonji pravac prikazuje reakciju bez inhibitora , srednji s malo inhibitora , a gornji s mnogo inhibitora . Kod c crtkani pravac vrijedi za normalnu reakciju bez inhibicije supstratom .
Komercijalni enzimi u preradi voća i povrća
Poznavanje osobina i načina djelovanja , kao i uslova za optimalno dejstvo fermenata , veoma je značajno za pravilno vodjenje tehnološkog postupka . Fermenti su redovni sastojci sirovine – svježeg voća i povrća i njihova aktivnost u periodu poslije berbe može da bude veoma štetna za kvalitet ovog polaznog osnovnog materijala , pa prema tome i za kvalitet gotovog proizvoda , ali se isto tako aktivnost ovih katalizatora može i veoma korisno da upotrijebi .
Izdvajanjem i koncentrisanjem prirodno sadržanih fermenata iz biljnog tkiva ili mnogo češće iz odredjenih vrsta mikroorganizama dobijaju se enzimatični preparati . Ovi preparati se razvojem tehnologije nalaze sve širu i veoma korisnu primjenu . Upotrebljavaju se za intenziviranje biohemijskih procesa koji se normalno odvijaju u biljnom tkivu ali teku veoma sporo , ili za obavljanje procesa koji sa berbom voća i povrća prestaju a neophodni su da se dobije proizvod odredjenog kvaliteta . Od enzimatičnih preparata koji se proizvode industrijskim putem poznati su : pektolitički , proteolitički , amilolitički zatim celulaza , katalaza , invertaza , glukozo-oksidaza i još neki drugi . Najširu primjenu u industrijskoj preradi voća i povrća imaju pektolitički enzimatični preparati . Upotrebljavaju se za bistrenje voćnih sokova , a isto tako za povećanje prinosa pri cijedjenju izdrobljenog voća i povrća . Dobijaju se u obliku praha kao i u obliku tečnih koncentrata.
Amilaze. Amilolitički enzimatični preparati ( amilaze ) se upotrebljavaju za hidrolizu škroba u proizvodnji dječije hrane na bazi cerealija , kao i u industriji vrenja , gdje škrob služi kao osnovni supstrat za fermentaciju . Zajedno sa pektolitičkim fermentima koriste se za bistrenje sokova . U proizvodnji škrobnih sirupa ( glukozni sirup, glukozno-fruktozni sirup ) hidroliza škroba može da se vrši primjenom enzima kao i kiselina . Hidroliza pomoću enzimatičnih preparata daje sirupe određenih svojstava . Takav sirup se manje lijepi i ima bolja reološka svojstva jer sadrži manje glukoze a više maltoze . Enzimatičnim preparatom može da se utiče na reakcije koje dovode do umanjenja gorčine proizvoda od grejfurta i pomorandže i za inverziju saharoze . Nakon poboljšanja tehnologije postupkom predhodnog namakanja (likvefakcije) škroba i uvođenjem termostabilnih enzima , otvorilo se novo područje rada ; pomoću enzima glukoza izomeraze , dobivena je paleta šećera medju kojima je dragocjena fruktoza , koja uz istu kalorijsku vrijednost ima gotovo dvostruku slatkoću u odnosu na glukozu. Uzimajući u obzir činjenicu da je šećer iz trske ili repe znatno skuplji od škroba iz krompira , ne treba obrazlagati šta to znači u proizvodnji sokova za masovnu upotrebu. Nadalje ne treba objašnjavati da se tako može proizvoditi alkohol , sorbitol pa i C vitamin .
Pektinaze. Pektolitički enzimi su oni koji kataliziraju hidrolizu pektinskog materijala . Kompletna hidroliza ima kao produkt pektinsku kiselinu . Pektinske supstance se mogu naći u osnovi tkiva posebno u voću . Ponekad pektinski enzimi javljaju se na više voća , a komercijalni enzimi se dobijaju iz plijesni Aspergillus niger . Komercijalni enzimi su mješavina od pojedinih pektičkih enzima , posebno pektin-metil-esteraza i poligalakturonaze. Sažeta direktna primjena ovih enzima je bistrenje soka i povećanje prinosa soka iz ploda . Tako pektolitički enzimi su važni za proizvodnju koncentrata voćnog soka i pirea . Da bi se dobio bistri sok mora se u toku proizvodnje izvršiti potpuna depektinizacija pomoću pektolitičkih enzima . Pektolitički enzimi se isto tako koriste za regeneraciju i stabilizaciju citrus ulja koja se dobiju iz kore narandže i limuna .
Proteaze. Proteolitički preparati ( proteaze ) nalaze daleko širu primjenu u industriji mesa i preradi mlijeka. U biljnoj preradi njihovim dejstvom postiže se veći stepen rastvorljivost proteina.Razlaganjem proteina i istovremeno razlaganje pektinskih materija , sokovi se bistre. Zamućenje u sokovima može da nestane i usljed naknadnog povezivanja bjelančevina što se vrlo uspješno spriječava dodatkom proteolitičkih enzima. Proteinaze tj. protein-hidrolizni enzimi se široko koriste u prizvodnji hrane ali su još uvijek novina u proizvodnji bistrih sokova. Proteolitični enzimi različitog porijekla i načina djelovanja se korisite u tretiranju brašna i tijesta; za tretiranje pšenice, kazeina iz mlijeka, ribe i sojinog proteina, kostiju i mesnog otpada kao i za zrijuće sireve.
Za proizvodnju bistrog soka neophodno je pronaći preteinaze koje se same izdvajaju od konvencijalnih po sledećim osobinama:
– pH je na optimalnoj vrijednosti između 3 i 4
– Mehanizam aktivnosti odgovara proteinu soka
Šta više, ove posebne proteinaze imaju funkciju da preferencijalno hidroliziraju one nisko težinske molekularne frakcije koje su odgovorne za mutnoću kod proizvodnje bistrog soka. Brojni istraživački projekti na univerzitetima u USA, kao npr. u Oregonu, su pokazali da su proteinaze vrlo pogodne za bistre sokove
. Specijalni enzimski proizvodi koji su razvijeni nakon procjene ovakvih projekata su dokazali da u spravaljnju bistog soka od jagodičastog voća određene prednosti se postižu:
– poboljšanje boje i stabilnost iste a prinos se da povećati izmedju 20% i 50%
– povećan kapacitet filtriranja povećanjem odnosa flux-a
– organoleptičke sposobnosti
Ostali enzimi. Celulaza je enzimatični preparat relativno novijeg datuma . Vrši hidrolizu celuloze prema reakciji
Celuloza ⎯⎯celulaza⎯→ celulozni dekstrin + glukoza
Optimum djelovanja ovog enzima je pH 3.5 mada ispoljava dosta zadovoljavajuću aktivnost u širokim granicama izmedju pH 2.5 do pH 8.0 . Temperaturni optimum je oko 50 0C . Primjenom ovog enzima može da se poveća svarljivost nekih vrsta povrća koje sadrže veće količine celuloze . Tako se omekšavanje i bolja svarljivost primjenom celulaze može postići kod prezrelih mahuna boranije kao i kod graška. U proizvodnji sokova od voća i povrća primjenom ovog preparata može da se postigne veći prinos , kao i razgradnja fino dispergovanih celuloznih sastojaka što doprinosi boljoj stabilizaciji soka . Ima pokušaja da se primjenom celulaza čvrsto tkivo prevede u tečno odnosno kašasto stanje.
Od oksidaza gluko-oksidaza i katalaza mogu da se primjene u preradi voća i povrća u odredjene svrhe . Uklanjanje kiseonika iz proizvoda pakovanih u hermetički zatvorenu ambalažu , postiže se korištenjem ovih fermenata. Učešćem ovih fermenata nastaju oksidacione reakcije čime se vezuje prisutan kiseonik .
2 H2O + O2 ⎯⎯katalaza⎯→ 2 H2O2
2 C6H12O6 + H2O2 ⎯⎯gluko⎯oksidaza⎯→ 2 C6H12O7 + 2 H2O
Gluko-oksidaza se dobija iz plijesni Pencillium glaucum, Aspergillus niger, Aspergillus oryzae i dr . Ona je specifičan ferment oksidiše glukozu do glukuronske kiseline . Primjenom oksidacionih enzimatičnih preparata zamjenjuje pakovanje proizvoda sa inertnim gasom, kao što je azot ili ugljendioksid. Vezivanjem kiseonika sprečavaju se oksidacione reakcije, koje bi mogle negativno da utiču na kvalitet i sastav proizvoda .
Za dehidrisane proizvode podložne oksidacionim promjenama pri pakovanju u hermetički zatvorenu ambalažu primjenjuju se specijalno pripremljeni enzimatični preparati u kesicama. Materijal od kojih su kesice izradjene propušta kiseonik a ne propušta nastalu vodu. U kesice se stavlja glukoza i enzimatični preparat sa podešenim optimalnim uslovima njegovog djelovanja. Kiseonik nesmetano prolazi u unutrašnjost kesice tako da se aktivni molekularni kiseonik utroši već poslije 24 časa od zatvaranja ambalaže . Interesantno je napomenuti da je prema nekim rezultatima ispitivana u proizvodnji kaše od jagoda , postignuto vrlo dobro očuvanje boje dodatkom ovog enzimatičnog preparata. Dobri rezultati su dobijeni i dodatkom gluko-oksidaze u majonezu . Preparat za poboljšanje ukusa: sušeni proizvodi kao i proizvodi konzervisani toplotom lako gube izvjesnu količinu sastojaka koji su nosioci karakterističnog ukusa. Da bi se ova svojstva regulisala mogu se dodavati enzimatični preparati, čime se postiže naknadno nastajanje ovih sastojaka. Tako se pokazalo da dodavanjem enzimatičnog preparata dobijenog iz biljaka familije krucifera, regenerišu se ukus i miris sušenog kupusa, celera, peršuna , spanaća , mrkve, crnog luka, konzerviranih jagoda i dr.
Enzimsko posmeđivanje
Tokom čuvanja i prerade prehrambenih proizvoda dolazi do različitih, poželjnih ili nepoželjnih, promjena boje. Ovim promjenama je posebno podložno voće i povrće. Promjena boje (posmeđivanje) do koje dolazi za vrijeme prerade i čuvanja voća i povrća ili proizvoda od voća i povrća može biti enzimsko i neenzimsko. U biljnom tkivi prisutni su tzv. autohtoni enzimi kao sastavni dio mezoplazme, plastida, mitohondrija i mikrozoma žive stanice. Endogeni (autohtoni) enzimi mogu imati korisne i štetne posljedice djelovanja, a oni imaju utjecaja na:
– starenje i kvarenje voća i povrća nakon branja;
– oksidaciju fenolnih supstanci fenolazom, što dovodi do tamnjenja – posmeđivanja;
– razgradnju pektinskih tvari nakon berbe, što vodi ka omekšavanju za vrijeme sazrijevanja.
Voće i povrće tokom transporta, skladištenja i konzerviranja dolaze u dodir sa brojnim materijama koje ne ulaze u njihov sastav. Gotovo je neizbježan kontakt sa kisikom iz zraka. Pri tome može doći do oksidacije spojeva koji su podložni oksidaciji. Kisik može biti prisutan i u biljnom tkivu ili može nastati kao produkt njegovog raspadanja. Oksidativni procesi nisu poželjni jer dovode do destrukcije biološke ili nutritivne vrijednosti voća i povrća Pored kisika i tragovi metala s kojima dolaze u kontakt voće i povrće mogu izazvati nepoželjne reakcije. Tragovi metala se javljaju kao ostaci sredstava za zaštitu bilja, a mogu da potječu i od opreme koja se koristi tokom konzerviranja ili od ambalaže. Promjene uzrokovane kisikom i tragovima metala najčešće su nepoželjne. Odražavaju se na promjene u boji, ukusu i aromi, što smanjuje prehrambenu vrijednost, a u određenim slučajevima mogu djelovati toksično na čovjeka (Cu, As).
Općenito, oksidacije u voću i povrću mogu se svrstati u:
autooksidacije (bez katalizatora),
oksidacije katalizirane metalnim ionima i
oksidacije katalizirane enzimima.
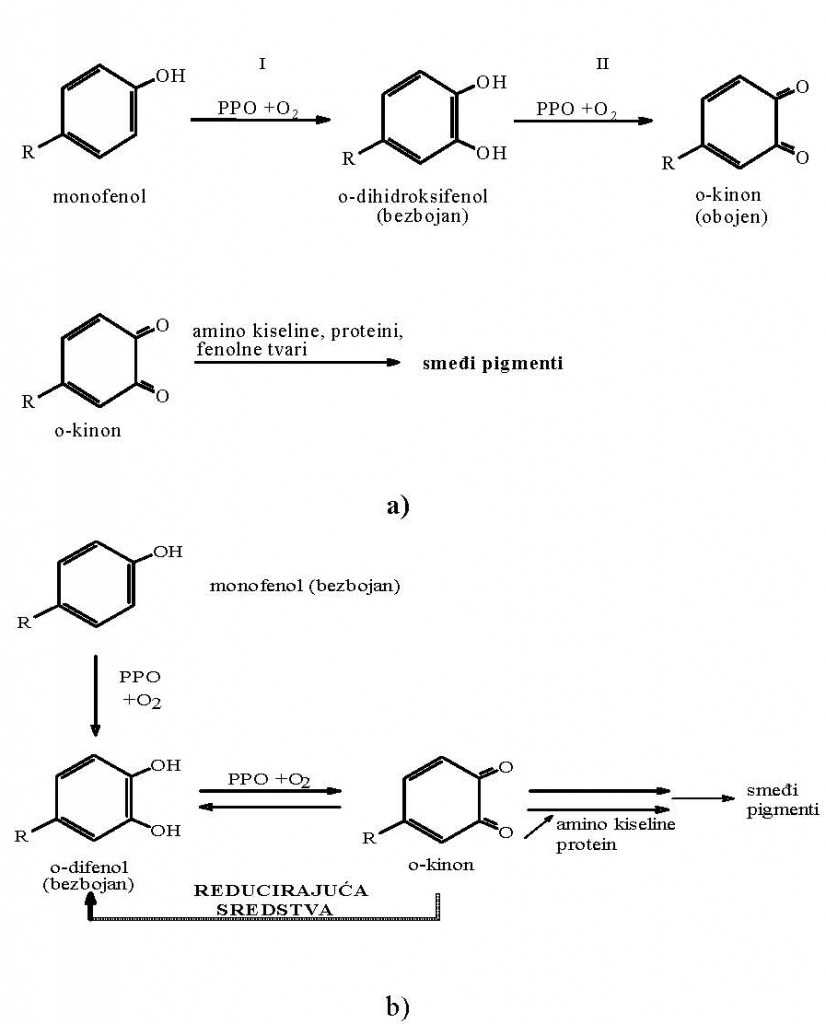
Oksidacije bez enzima (autooksidacije) odvijaju se dosta sporo. Za opažanje promjena potrebno je da prođe nekoliko sati, dana ili sedmica. Oksidacije katalizirane enzimima odvijaju se veoma brzo, a nepoželjne promjene boje mogu se zapaziti u vremenu od nekoliko minuta do nekoliko sati. Nepoželjni oksidativni enzimski procesi započinju nakon oštećenja ili uništenja žive stanice. Tom prilikom dolazi do narušavanja normalne ravnoteže enzima i do njihove dezorganizacije u stanici. Nepoželjni oksidacioni procesi u zdravoj živoj stanici ne dolaze do izražaja. Kod enzimskog posmeđivanja voća i povrća, kao i njihovih prerađevina, najznačajniji je enzim polifenoloksidaza. Ovaj enzim pripada tirozinazi (monofenol monooksigenaza; polifenoloksidaza, kateholoksidaza, kisik oksidoreduktaza). Sadrži bakar kao prostetsku skupinu, a poznat je pod drugim imenima kao npr. katehol oksidaza, o-difenolaza, fenolaza i polifenoloksidaza (PPO). Tirozinaza je široko zastupljen enzim koji ima ključnu ulogu u biosintezi melanina i ostalih polifenolnih spojeva. Ovaj enzim katalizira
ortohidroksilaciju monofenola do o-difenola (krezolazna ili monofenolazna aktivnost i
oksidaciju o-difenola do o-kinona (kateholazna ili difenolazna aktivnost)
Mikroorganizmi i biljke sadrže veliki broj strukturno različitih monofenola, difenola i polifenola koji su supstrati tirozinazi. Budući da su mnoge biljke bogate polifenolima, a pojava enzimskog posmeđivanja uglavnom vezana za njih to se za ovaj enzim najčešće koristi ime polifenoloksidaza (PPO).
Hemizam enzimskog posmeđivanje. Enzimsko posmeđivanje je značajan problem kod brojnih važnih proizvoda od voća i povrća. Ova pojava posebno je izražena kod voća kao što je jabuka, kruška, breskva, banana i povrća: krompir, gljive, leguminoze. Također je prisutna kod nekih plodova mora. Enzimsko posmeđivanje predstavlja negativnu pojavu koja je vezana za promjenu boje i sastava voća i povrća kojemu je na bilo koji način narušena osnovna struktura (guljenje, rezanje, drobljenje…), ili stanje ravnoteže. Promjena boje (posmeđivanje) svježeg voća, povrća i proizvoda od voća i povrća je kompleksan proces tokom kojeg se monofenolni spojevi, uz prisustvo polifenoloksidaze i kisika, hidroksiliraju u odifenole, koji se kasnije oksidiraju do o-kinona. Nastali kinoni su jako reaktivni i u neenzimskim reakcijama sa fenolnim spojevima, amino kiselinama, itd. daju smeđe do crno obojene melanoidne pigmente. Za sve ove procese je zajedničko da započinju kontaktom između fenolnih spojeva (pretežno smještenih u vakuolama) i enzima (smještenih u citoplazmi), koji stupaju u kontakt tek kada je narušena stanična struktura.
Najčešći supstrati za kateholaze i lakaze su spojevi: katehol, 4- metil katehol, DOPA, kinol, klorogenska kiselina, tolukinol, katehin. Supstrati koji podliježu enzimskom posmeđivanju: katehin, flavon, klorogenska kiselina, kvercetin, kafa kiselina, katehol. Enzimsko posmeđivanje je promjena boje koja nastaje kada se monofenolna jedinjenja u prisustvu atmosferskog kisika i polifenoloksidaze (PPO) transformiraju u o-difenole, a kasnije oksidiraju do kinona. Polifenoloksidaze (PPO) su također poznate kao tirozinaze, o-difenol oksidaze, katehol oksidaze, itd. U drugom stupnju kinon se kondenzira i reagira neenzimski sa drugim fenolnim komponentama, aminokiselinama, itd. i proizvodi pigmente, kompleksne mrke polimere. Varijeteti fenolnih spojeva se oksidiraju sa PPO, a najvažniji supstrati su katehini, 3,4- hidroksifenilalanin (DOPA) i tirozin. Optimalni pH za aktivnost PPO je između 5 i 7.
Enzimsko posmeđivanje se promatra kao oks-redoks biohemijski proces. Oksidacija polifenola predstavlja oksidaciju (dehidrogenaciju) brojnih jedinjenja biljnog tkiva, uglavnom voća, koja sadrže tipična jedinjenja koja po strukturi odgovaraju jedno ili viševalentnim fenolnim spojevima. Oksidacijom ovih jedinjenja dolazi do promjena na tkivu voća i povrća. Pri tome su najčešći donori vodika jedinjenja tipa o-difenola (katehol). Pod utjecajem katalizatora (enzima PPO) ova jedinjenja se vrlo brzo oksidiraju i nastaju kinoni, koji su reaktivni, lako se polimeriziraju u kompleksne spojeve koji su mrko obojeni. Prirodni katalizator enzim polifenoloksidaza (PPO) djeluje poslije mehaničke dezintegracije tkiva, odnosno tek tada proces i može da se zapazi. Ovaj enzim, kao i većina drugih enzima, koncentrirani su u plastidima stanice, i dok stanica nije oštećena, on nije u kontaktu sa polifenolima koji su rastvoreni u staničnom soku. Polifenoldksidaza učestvuje zajedno sa citokromoksidazom u procesu disanja (u prijenosu vodikovih iona).
a) hemijske reakcije tamnjenja b) reakcije redukcije
Ako se radi o dezintegriranim biljnim dijelovima, utvrđeno je da do tamnjenja soka, pogotovu jabučastog voća, u većoj mjeri dolazi ako su prisutne i čestice jestivog dijela (tkiva). Ukoliko se ovakav sok oslobodi ovih dijelova (npr. profiltrira), u takvom soku će u istom vremenu doći do slabijeg tamnjenja. U slučaju polifenoloksidaze dolazi do samoinhibicije, tj. aktivnost ovog enzima vremenom opada. Iako duže djelovanje ovog enzima prouzrokuje veće tamnjenje, značajni su rezultati koji pokazuju da se kinonski oblici polifenola ili polimerizirani kinoni apsorbiraju na jedinjenja u čiji sastav ulazi azot. U tom slučaju se formira teško rastvorljiv kompleks melanina i azotnih jedinjenja koji se filtriranjem može odvojiti, nakon čega sok postaje svjetlije boje. Ovaj fenomen je našao primjenu u praksi.
Mrko obojeni dijelovi na jabukama i drugim plodovima mogu se pojaviti uslijed mehaničkog pritiskivanja i gnječenja, a bez povrede pokožice. U ovom slučaju polifenolne materije koje se nalaze u staničnom soku dolaze u dodir sa zrakom, koji se nalazi u međustaničnim prostorima, dolazi do oksidacije polifenola, odnosno do pojave tamnih polja. Slično se događa i pri zamrzavanju plodova kada biljne stanice uginu, vazduh slobodno prolazi kroz staničnu membranu i u dodiru sa staničnim sokom oksidira prisutne polifenole. Otuda su obično plodovi koji su bili smrznuti tamnije obojeni a istovremeno zbog oksidacije polifenolnih jedinjenja postaju manje trpki.
Do posmeđivanja prirodnih obojenih materija fenolnog karaktera (antocijana) može doći bilo da oni sadrže jednu, dvije ili tri fenolne grupe. Pirogalol (trihidroksifenol) se također oksidira; njegove oksidacione forme reagiraju sa bojenim i taninskim materijama, pa može doći do formiranja nerastvorljivih kompleksa koji se izdvajaju u vidu taloga. Ovakva oksidacija se pogotovu odvija u vinima koja su dobijena od grožđa zaraženog tzv. plemenitom truleži. Ova »trulež« sadrži enzim lakazu, koji djeluje isto kao polifenoldksidaza ali je od nje mnogo otpornija prema spoljašnjim činiocima. Gubitak boje ograničava rok trajanja mnogih minimalno procesiranih proizvoda, a također može biti problem kod dehidriranog i smrznutog voća i povrća. Kinoni se lako polimeriziraju a isto tako se lako jedine sa amino-grupama, tiolnim grupama i metilenskim grupama amino kiselina. Zbog toga se tiamin, metionin i lizin djelomično jedine sa nastalim o-kinonima, uslijed čega je namirnica manje vrijedna sa nutritivnog aspekta. Sličan karakter oksidoredukcije se dešava i u nepovrijeđenom ali prezrelom tkivu, kada dolazi do dezorganizacije dotadašnjih procesa koji su još potpomognuti proizvodima intramolekularnog disanja, kao što su etilen, alkohol, acetilen, i dr.
Enzimsko posmeđivanje nije uvijek greška na proizvodu. Ova diskoloracija učestvuje u reakcijama formiranja boje kod rozina, šljiva, kafe, čaja, kakaoa.
Supstrati enzimskog posmeđivanja Za odvijanje procesa enzimskog posmeđivanja neophodno je prisustvo određenog supstrata na kojeg djeluju enzimi. Supstrati PPO u reakcijama enzimskog posmeđivanja su monofenoli, odnosno difenoli sa hidroksilnim skupinama u orto položaju, odnosno u para položaju.
Fenolni spojevi su važni za postizanje arome i boje proizvoda od voća i povrća (sokovi, vina). Zahvaljujući svojim antioksidativnim svojstvima imaju antikancerogeno djelovanje, a neki zbog mehanizma zaštite od oksidacije pojedinih lipoproteina, sprječavaju oboljenja srca. Fenolni spojevi, također, mogu imati i negativan učinak, osobito kod proizvoda od voća i povrća (sokovi, vina, minimalno procesirano voće i povrće) gdje mogu sudjelovati u tvorbi nepoželjnih taloga, odnosno žutih i smeđih pigmenata. Boja, trpkost, gorčina (gorkost) i aroma su svojstva koja ovise o sadržaju fenolnih tvari.
Sprječavanje enzimskog posmeđivanja
Da bi se uspješno spriječilo enzimsko posmeđivanje hrane potrebno je voditi računa o uzrocima koji do njega dovode, a to su
• enzim,
• supstrat
• kisik.
Zbog toga se i načini sprječavanja posmeđivanja dijele prema tome na koji se od ovih činilaca djeluje.
I Djelovanje na enzim (PPO) .Postoji više načina djelovanja na PPO u cilju sprječavanja enzimskog posmeđivanja. Enzimsko posmeđivanje može biti kontrolirano u nekom voću i povrću blanširanjem pri čemu se inaktivira PPO. Ovo je najpoznatiji i najčešće primjenjivani postupak inaktiviranja enzima. Djelovanje topline se ogleda u promjenama u sekundarnoj i/ili tercijarnoj strukturi molekule enzima, čime se utječe na katalitičku aktivnost Međutim, sama primjena visokih temperatura povezana je sa negativnim promjenama arome, teksture i boje proizvoda te se ne može koristiti u svim slučajevima pripreme hrane (npr. pri proizvodnji minimalno procesirane hrane). Učinak topline na aktivnost PPO je veoma različit obzirom na izvor PPO.
Budući da uslijed termičkog tretiranja hrane dolazi do znatnih promjena organoleptičkih svojstava, odnosno njenog sastava, sve više se radi na iznalaženju metoda konzerviranja gdje bi se reducirala primjena topline. To su metode u kojima se kombinira utjecaj topline, ultrazvuka i povišenog tlaka na aktivnost polifenoloksidaze. Učinak ultrazvuka na enzimsku aktivnost znatno raste sa porastom amplitude ultrazvučnih valova: vrijeme decimalne redukcije, pri konstantnoj temperaturi opada logaritamski sa porastom amplitude. Djelovanje sa tvarima koje snižavaju pH – askorbinska kiselina, limunska kiselina, jabučna kiselina, vinska kiselina, itd. Reakcije s tvarima koje stvaraju komplekse sa bakrom kao aktivnim središtem – halidi; cijanidi; CO2; natrij dietilditio-karbamat; azidi; mimozin*; aminokiseline, peptidi, proteini*; kojična kiselina; H2O2; alkoholi. Reakcije sa spojevima strukture slične supstratima – tropolon, 4- heksilrezorcinol, aromatske kiseline. Ostalo λ-karagenan, sam ili u kombinaciji sa limunskom kiselinom
II Djelovanje na supstrat . Za ovo se koriste slijedeća sredstva:
Reducirajuća sredstva – askorbinska kiselina, sulfiti, tiolne tvari.
Sredstva koja stvaraju komplekse sa međuproduktima – cistein; aminokiseline, peptidi i proteini.
Sredstva koja djeluju na supstrate – ciklodekstrini.
Ostalo – polietilen glikol, Sephadex, polivinilpirolidin metiliranje jedne ili više hidroksilnih grupa na fenolnom supstratu, korištenje meda, itd.
III Djelovanja na kisik. Pošto je jedan od uvjeta nastanka posmeđivanja prisustvo kisika da bi se sprječilo nastajanje smeđe boje treba ukloniti uzrok koji dovodi do njenog nastanka. To znači da treba ukloniti kisik, a to se može uraditi na više načina. Neki od njih su potapanje svježeg voća i povrća u vodu ili u otopine kiselina (limunske, askorbinske), otopinu šećera ili kuhinjske soli, pakiranje u vakuumu, u modificiranoj atmosferi, itd.
Neenzimsko posmeđivanje
Jedan od čestih fenomena u hemiji prirodnih proizvoda od voća i povrća, koji se javljaju u toku pripreme, prerade i skladištenja je neenzimsko tamnjenje. Nasuprot reakcijama tamnjenja koje uključuju djelovanje enzima, ove reakcije ne zahtijevaju enzimsko katalitičko djelovanje. Reakcije neenzimskog tamnjenja praćene su razvijanjem arome, izmjenom tkiva i javljanjem žute, crvene, mrke i crne boje. To proizvod čini više ili manje prihvatljivim za potrošača, ali u svim slučajevima hranjiva vrijednost biva djelomično izmijenjena. Reakcije neenzimskog tamnjenja obuhvataju različite vrste reakcija: dehidrataciju, degradaciju, fragmentaciju, kondenzaciju i polimerizaciju čiji su hemizmi i kinetika kompleksni. Neenzimsko posmeđivanje (tamnjenje) u velikom broju slučajeva predstavlja negativnu pojavu koja dovodi ne samo do promjene boje nego i drugih promjena kao što su degradacija sastojaka hrane (aminokiseline, askorbinska kiselina), smanjenje probavljivosti proteina, a u nekim slučajevima dovodi i do tvorbe toksičnih spojeva. Neenzimsko posmeđivanje obuhvata čitav niz reakcija koje dovode do tvorbe smeđih pigmenata. Međutim, neenzimsko posmeđivanje ne predstavlja uvijek negativnu pojavu, te se često radi na stvaranju uvjeta da do njega dođe. Produkti neenzimskog posmeđivanja su spojevi određene boje i arome koji su u nekim slučajevima poželjni i veoma bitni za prihvaćanje nekih proizvoda od strane potrošača (pekarski proizvodi, pečeno meso, pržena kafa, čips itd). Spojevi nastali u tim reakcijama su važni sastojci arome mliječne čokolade, a također važnu ulogu imaju i pri proizvodnji karamela, mliječnih bombona i drugih slatkiša.
Hemizam reakcija neenzimskog tamnjenja
Kada se reakcije neenzimskog tamnjenja odvijaju bez prisustva azotnih jedinjenja, ove reakcije se označavaju kao reakcije karamelizacije, a kada se odvijaju u prisustvu azotnih jedinjenja one se nazivaju karbonil – amin reakcije ili Maillard reakcije.
Reakcije karamelizacije. U mnogima slučajevima, mada to ne mora biti, šećeri su osnovni reaktanti u reakcijama karamelizacije. Ove reakcije obuhvataju transformaciju i degradaciju šećera bez prisustva amino-jedinjenja. Pod anhidriranim (bez vode) uvjetima zagrijavanja ili pri visokim koncentracijama šećera u razblaženim kiselim rastvorima, inicijalni stupnjevi reakcije karamelizacije su karakterizirani nastajanjem anhidrošećera. Proces karamelizacije obuhvata reakcije: enolizacije, izomerizacije, dehidratacije, fragmentacije i polimerizacije pri čemu se grade pigmenti svijetlo žute do crne boje. Prilikom karamelizacije saharoze na 200 °C utvrđena su tri endotermna procesa. Poslije topljenja saharoze započinje pjenušanje mase i dolazi do gubitka jedne molekule vode po molekuli saharoze što dovodi do formiranja izosakrozana. Daljim zagrijavanjem uz gubitak mase nastaje karamelan (C24H36O18). Izolirani karamelan rastavara se u vodi i etil–alkoholu i ima gorak ukus. Treći stupanj se javlja poslije pjenušanja, dužim zagrijavanjem i gradi se pigment karamelen. Njegova prosječna molekulska masa odgovara gubitku osam molekula vode iz tri molekula saharoze :
3C12H22O11 → C36H50O25 + 8 H2O
Dehidratacija saharoze
Dalje zagrijavanje saharoze dovodi do formiranja humina, odnosno karamelina, tamne supstance visoke molekulske mase C125H188O80. Humini (šećer-karameli) pored hidroksilnih grupa različite baznosti, karboksilne i enolne grupe često imaju prisutne fenolne hidroksilne grupe.na taj način se može objasniti pojava da ioni nekih metala intenziviraju boju karamel-pigmenata. Mehanizam nastajanja karamel pigmenata uključuje reakciju polimerizacije pri čemu se dobijaju obojeni polimeri visoke molekulske mase, u kojima se broj C atoma proporcionalno povećava stupnju dehidratacije, odnosno visini temperature i dužini njenog djelovanja. To u sistemima koji podliježu reakcijama karamelizacije vodi drugim, paralelnim reakcijama vrlo kompleksnog mehanizma i nastajanju crvenih, mrkih i tamno-mrkih pigmenata različitog sastava i osobina, koji se znatno i po strukturi i po sastavu i po osobinama razlikuju od aldo karamela.
Karbonil – amin reakcije. Neenzimsko posmeđivanje je jedan od najpoznatijih uzroka destrukcije koji nastaje za vrijeme skladištenja osušenih i koncentriranih prehrambenih proizvoda. Neenzimsko tamnjenje ili Maillardove reakcije mogu biti podijeljene u tri razine:
a) rane reakcije koje su hemijski dobro definirani korak u kome ne dolazi do tamnjenja,
b) napredne Maillard-ove reakcije koje vode ka formiranju nepoželjnih rastvorljivih supstanci i
c) finalne Maillard-ove reakcije koje dovode do stvaranja nerastvorljivih smeđih polimerima.
Jedna od reakcija koja dovodi do neenzimskog posmeđivanja je reakcija između reducirajućih šećera, većinom D-glukoze, i slobodnih aminokiselina ili slobodnih amino skupina na proteinskim lancima.Ovi procesi su prisutni kod termičkog tretmana životnih namirnica: sušenje, pečenje, prženje, itd. Reakcioni prekursor je:
Amino sastav + reducirajući šećer (karbonil grupa) —> (promjena arome i boje)
Ako se aldoze ili ketoze zagrijavaju u otopini sa aminima (amini i amino grupe, aminokiselina ili drugih amino jedinjenja) dolazi do stvaranja velikog broja spojeva različite boje i arome
Osnovni hemijski mehanizam neenzimskog tamnjenja
Reducirajući šećeri reagiraju reverzibilno sa aminima, dajući glikozilamine pa je početni kondenzacioni proizvod N-supstituirani glikozilamin. Reakcijom nazvanom Amadorijevo premještanje, u slučaju D-glukoze, dolazi do nastanka 1-amino-1-deoksi-D-glukoze. Nastali produkt se dalje transformira, osobito pri nižim pH vrijednostima (niže od 5), pri čemu nastaju različiti intermedijeri, do konačnog spoja, koji je u slučaju heksoza 5-hidroksimetil-2- furaldehid (HMF). U slučaju viših pH vrijednosti (iznad 5), reaktivni ciklični spojevi (HMF i drugi) polimeriziraju brzo do tamno obojenih, netopljivih spojeva koji sadrže dušik.
U inicijalnim stupnjevima reakcije između aldoza i ketoza s aminokiselinama moguće je nastajanje i sekundarnih proizvoda neenzimskog tamnjenja, koji mogu biti čak i rektivniji od primarnih proizvoda. Na primjer, ketozil-amin može reagirati s novom molekulom aldoze dajući diketozilamin, a aldozilamin također može reagirati sa molekulom amina dajući diamino šećere. Dok je inicijalni stupanj reakcije između aldoheksoza ili ketoheksoza i aminokiselina karakteriziran monomolekulskom reakcijom adicije, dalji stupnjevi mogu izmijeniti odnos reaktanata u proizvodnji i to na više načina. Različit redoslijed pojedinih faza reakcije neenzimskog tamnjenja su utvrđeni kao međuproizvodi reakcije.
Sa stvaranjem 1,2 – dienolnih oblika aldozilamina i ketozilamina, reakcija dalje degradacije i kondenzacije dovodi do pojave žutomrke boje reakcione smjese. Redoslijed nastajanja mrkih pigmenata u reakcijama između aldoza i ketoza sa amino kiselinama je sličan, u mnogim slučajevima, stvaranju karamel-pigmenata u reakcijama karamelizacije. Međutim, za razliku od pigmenata nastalih u reakcijama karamelizacije, ovi pigmenti u svojim molekulama sadrže atom ili atome azota i nazivaju se općim imenom melanoidini. Pokušaji da se dobije standard melanoidina nisu bili uspješni jer sastav pigmenata zavisi, u svim slučajevima, od prirode reaktanata, pH sredine, temperature i vremena trajanja same reakcije.
Faktori koji utječu na reakciju tamnjena
U većini slučajeva nije moguće raspravljati bilo koji konstantan efekat u reakciji neenzimskog tamnjenja, a da se ne vodi računa o ponašanju reakcije pod utjecajem i ostalih parametara. Značajni parametri u reakcijama neenzimskog tamnjenja su: temperatura, pH sredine, aw (aktivnost vode), priroda i koncentracija reaktanata, vrijeme trajanja reakcije i sadržaj vode. Zavisno od ovih činilaca reakcija se odvija sa različitim kvalitativnim promjenama i različitim brzinama.
Temperatura. Ovisnost reakcije o temperaturi često se izražava putem energije akivacije (Ea). Podaci o energiji aktivacije za Maillard-ove reakcije su u dijapazonu od 10-160 KJ/molu, u zavisnosti koji je efekt od koje reakcije bio mjeren. Energija aktivacije vrlo je ovisna o pH, strukturi reaktanata pa je teško izolirati efekt temperature kao samostalnu varjablu. Kod svihmodel sistema, brzina tamnjenja, mjerena razvijanjem boje, povećava se dva do tri puta za svakih 10 °C povećanja temperature. Za prirodne sisteme kao što je npr. krompir sa visokim sadržajem šećera i amino kiselina, brzina tamnjenja je mnogo veća i može dostići eksplozivni obim. Npr. razlaganje fruktoze se povećava pet do deset puta za svakih 10 °C povećanja temperature. Ako se temperatura povećava nastaju jedinjenja koja se mogu uključiti u reakcije tamnjenja ili ih inhibirati. Saharoza je inertna pri relativno niskim temperaturama, ali kada uvjeti reakcije budu pogodni za njenu hidrolizu u glukozu i fruktozu, novonastala jedinjenja se vrlo lako uključuju u rekcije karamelizacije ili u karbonil – amin reakcju. Aminokiseline kataliziraju reakciju saharaoze pri neutralnim pH vrijednostima, dok formaldehid koji nastaje Streckerov-om degradacijom glicina može efektno blokirati učešće neizreagiranog glicina ili ostalih aminokiselina u reakciji neenzimskog tamnjenja.
pH vrijednost. Promjena pH vrijednosti nekog model sistema vodi kvalitativno različitim reakcijama tamnjenja. Reakcije tamnjenja pokazuju smanjenje brzine reakcije pri niskim pH vrijednostima, odnosno pH vrijednostima optimalne stabilnosti prisutnih reducirajućih šećera. Same reakcije tamnjenja imaju utjecaja na pH pa je zbog toga teško procjenjivati utjecaj pH na ukupan sistem. Reakcija karbonil jedinjenja i amino kiselina je samoinhibirajuća zbog činjenice da se smanjenjem pH vrijednosti reakcione sredine gubi baznost amino grupe. Ovakvi zaključci se rijetko mogu primijeniti na prirodne sisteme. Ispitivanje efekata pH na prirodu reakcije neenzimskog tamnjenja se komplicira činjenicom da komponente pufera mogu biti reaktanti u reakciji tamnjenja. Ispitivanja su pokazala da je kod vodenih rastvora tamnjenje posljedica karamelizacije, dok pri skoro suhom stanju reaktanata ili pri alkalnim pH vrijednostima, preovladavaju Maillard-ove reakcije.
Voda i koncentracija reaktanata. Voda katalizira enolizaciju reducirajućih šećera, a enolni oblici lako podliježu reakciji fragmentacije i dehidratacije. Na početku karbonil – amin reakcije aldoza ili ketoza šećer reagiraju sa primarnim ili sekundarnim aminom ili aminokiselinom dajući glikozilamin, pri čemu je reakcija reverzibilna. Utjecaj sadržaja vode je značajan za prinos glikozilamina. Pri niskim sadržajima vode nastaje značajno građenje ovih jedinjenja, zbog čega je karbonil – amin neenzimsko tamnjenje izraženo kod dehidriranih i koncentriranih prehrambenih proizvoda
Koncentracija reaktanata također utječe i na smjer reakcije, a prinos melanoidina se može povećati tri do pet puta kada se koncentracija reaktanata udvostruči. Brzina reakcije je maksimalna pri sadržaju vode od 30%, a minimalna ako je koncentracija vode 90% ili nula. Smanjenje u brzini reakcije pri sadržaju vode iznad 30% najvjerovatnije je izazvano razblaženjem reaktanata, dok od smanjenja brzine reakcije pri sadržaju ispod 30% dolazi zbog prijemljivosti šećera prema niskom aktivitetu vode.
Reaktivnost šećera u reakcijama neenzimskog tamnjenja je istovjetna njihovoj reaktivnosti u svim ostalim slučajevima. Pentoze su reaktivnije od heksoza. Nereducirajući disaharidi mogu učestvovati u reakciji poslije hidrolize na monosaharide. Unutar izomera kao što su aldopentoze ili aldoheksoze, reaktivnost je uvjetovana konformacionom stabilnošću favorizirane strukture hemiacetalnog prstena. Od aldopentoza koje se javljaju u prirodi L-arabinoza je aktivnija od D-ksiloze. Između aldoheksoze koje se javljaju u prirodi red reaktivnosti bi bio:
manoza > galaktoza > glukoza
Ovakvo ponašanje je slično njihovoj konformacijskoj stabilnosti, odnosno broju molekula otvorene strukture prisutnih u rastvoru. Reaktivnost aminokiselina u reakcijama neenzimskog tamnjenja zavisi od njene koncentracije, kao i od reaktivnosti aldehida nastalog degradacijom ispitivane aminokiseline.Neke aminokiseline imaju više od jednog reaktivnog azotovog atoma kojim učestvuje u karbonil – amin reakciji. Međutim, ne mora biti da je svaki strukturalni atom azota bezuvjetno reaktivan. Sa izuzetkom glutamina, α – amino grupe aminokiselina lako reagiraju sa aldehidima i ketonima. Vjerovatno je da amino grupa glutamina lako reagira, dajući pirilidonkarbonsku kiselinu, inertno heterociklično jedinjenje, u kojem je atom azota uključen u zatvoreni prsten. S druge strane, α – amino grupa asparagina je veoma reaktivna, dok je atom amidnog azota inertan. Atom α – amino azota i jedan od heterocikličnih N-atoma histidina su reaktivni u reakciji sa karbonilnim jedinjenjima na visokim temperaturama. Oba atom azota lizina su reaktivna, dok je kod arginina jedino atom α – amino azota sposoban za reakciju. Ako se amino grupa udaljava od α položaja na alifatični niz, ali ne u terminalni položaj, reaktivnost opada. Aminobuterna kiselina sa termalnom amino grupom pokazuje veću tendenciju učešća u karbonil-amin reakcijama u odnosu na svoje strukturne izomere.
Voda se izdvaja za vrijeme Maillard-ovih reakcija, pa ove reakcije pokazuju rapidan pad u hrani sa visokom aw, kao i kod niske aw jer je pri tome ograničena mobilnost reaktanata.
Mjere za sprječavanje reakcija neenzimskog tamnjenja
Sprječavanje neenzimskog posmeđivanja, u kompleksnom sustavu kakav je hrana, nije uvijek lako ostvariti. U jednom kompleksnom sistemu kao što je voće i povrće teško je predložiti opštu metodu za sprječavanje reakcija neenzimskog tamnjenja, mada se mogu samo inicirati neke mogućnosti, a primjena svake metode mora biti prosuđena prema proizvodima, manama i prednostima u svakom posebnom slučaju. Neki opći principi i metode za sprječavanje neenzimskog posmeđivanja su slijedeći:izbor sorti, uvjeti skladištenja i čuvanja, primjena odgovarajućeg procesa proizvodnje, primjena sulfita tamo gdje je dozvoljeno prema propisima, smanjenje količine amino spojeva ili proteina, smanjenje količine reducirajućih šećera itd.
Zaključci
Neenzimatsko posmedjivanje po svom hemizmu najčešće je bazirno na reakcijama karamelizacije i Millardovim reakcijama.Na intezitet promjene boje utiču različiti faktori kao što je temperatura, koncentracija reaktanata, aw , pH vrijednost i drugi.Ove reakcije nastaju pri tretiranju namirnica napovišenim, odnosno visokim temperaturam.
Literatura
1. Peterson, M.S., Johnson, A.H.: Encyclopedia of Food Science. The Avi publishing company, Inc., Vestport, Conneticut, 1978.
2. Paul, P.C., Palmer, H.H.: Food Theory and Applications. Joh
Wiley &Sons, Inc., 1972.
3. Potter, N.N.: Food science. The Avi publishing company, Inc.,
Vestport, Conneticut, 1978.
4. Canjura, F.L., Schwartz, S.J.: Separation of chlorophyll compounds and their polar derivatives by HPLC. J. Agric. Food Chem., 39, 1102-1105, 1991. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
5. Loef, H.W., Thung, S.B.: Ueber den Einfluss von Chlorophyllase auf die Farbe von Spinat waehrend und nach der Verwertung. Z. Lebensm. Forsh., 126, 401-406, 1965. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
6. Schwartz, S.J., Lorenzo, T.V.: Chlorophyll stability during aseptic processing and storage. J. Food Sci. 56, 1056-1062, 1991.
7. Jones, I.D., White, R.C., Gibbs E., Butler, L.S., Nelson, L.A.: Experimental formation of zinc and copper complexes of chlorophyll derivates in vegetable tissue by thermal processing. J. Agric. Food Chem., 25, 149-153, 1977. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
8. Tan, C.T., Francis, F.J.: Effect of processing temperature on pigments and color of spinach. J. Food. Sci., 27, 232-240, 1962.
9. Buckle, K.A., Edwards, R.A.: Chlorophyll: Color and pH changes in HTST processed green pea puree. J. Food Technol. 5, 173-186, 1979. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
10. Gross, J.: Pigments in Vegetables: Chlorophylls and Carotenoids, Van Nostrand Reinhold, New York, 1991. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
11. Perry, A.D., Horgan, R.: Abscisic acid biosythesis in roots: The identification of potential abscisic acid precursors, and other carotenoides. Planta 187, 185-191, 1992. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
12. Peiser, C.Y., Yang, S.F.: Sulfite-mediated destruction of β- karoten. J. Agric. Food Chem. 27, 446-449, 1979. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
13. Ben Aziz, A., Grossman, S., Ascarelli, I., Budowski, P.: Carotenbleaching activities of lipoxygenase and heme proteins as studied by a direct spectrophotometric method. Phytochemistry. 10, 1445-1452, 1971. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
14. Burton, G.W., Ingold, K.U.: Beta-carotene: An unusual type of lipid antioxidant. Science, 224, 569-573, 1984. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
15. Sies, H.: Antioxidant functions of vitamins: Vitamins E i C, betacarotene and other carotenoids. Ann. NY Acad. Sci. 669, 7-20, 1992. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
16. Davies, W.J., Zhang, J.: Root signals and the regulation of growth and development of plants in drying soil. Annu. Rev. Mol. Biol. 42, 55-76, 1991. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
17. Huang, A.S., Von Elbe, J.H.: Effect of pH on the degradation and regeneration of betanin. J. Food Sci. 52, 1689-1698, 1987.
18. Francis, F.J.: Antocyanins, Curent aspects of food colorants, CRC Press, Cleveland, OH, pp. 19-27, 1977. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
19. Markakis, P.: Stability of antocyanins in foods, in Antocyanins as Food Colors (P. Markakis, ed.), Academic Press, New York, pp. 163-180, 1982. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
20. Goodman, L.P., Markakis, P.: Sulfur dioxide inhibition of antocyanin degradation by phenolase. J. Food Sci. 130, 135-137, 1965. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996.
21. Pedreno, M.A., Escribano, J.: Correlation between antiradical activity and stability of betanine from L roots under different pH, temperature and light conditions. J. Sci. Food Arric. 81, 627-631, 2001. cit. u Von Elbe, J.H., Schwartz S.J.: Colorants in Fennema, O.R.: Food Chemistry. Marcel Dekker, Inc., New York, 1996
22. . 1. W. Fogarthy and C.T.Kelly, Microbial Enzymes and Biotechnology, Elsevier Applied Science, London and New York, 1990.
23. Biocatalysis in Organic Media, Proceedings of an International Symphosium organized under Auspices of the Working Party on Applied Biocatalysis of EFB, Wageningen, 7-10 Dezember 1986, Elsevier Science
24. W.Bains, Biotechnology from A to Z, Second Edition, Oxford, New York and Tokyo, Oxford University Press, 1998.
25. J.M.S.Cabral, D.Best, L.Boross and J.Tramper, Applied Biocatalysis, Harwood academic publishers, Switzerland, 1994.
26. D.Šubarić: Inhibicija polifenoloksidaze u svrhu sprečavanja enzimskog posmedjivanja,Doktorski rad ,Pregrambeno, 1999
27. http://www.hzjz.hr/zdr_ekologija/priopcenja/arome/podjela.htm
28. http://www.agsci.ubc.ca/courses/fnh/410/colour/3_70.html
29. http://www.agsci.ubc.ca/courses/fnh/410/colour/4_40.htm
30. http://www.agsci.ubc.ca/courses/fnh/410/colour/3_30.htm
32. http://fn.cfs.purdue.edu/bot/VideoConferencePres/Ferruzzi10-29- 02.pdf
33. http://www.agsci.ubc.ca/courses/fnh/410/colour/3_22.htm
34. http://metallo.scripps.edu/PROMISE/1MBO.html#Fig
35. http://metallo.scripps.edu/PROMISE/1BBB.html#Fig
36. http://www.codexalimentarius.net/gsfaonline/additives/details.html?id=21
37. http://europa.eu.int/eurlex/en/consleg/pdf/1995/en_1995L0002_do_001.pdf
40. www.cpkelco.com/pectin/gelling_mechanism.html
41. http://www.fao.org/docrep/W6864E/w6864e08.htm
42. www-personal.umich.edu/…/bio415/hex.1.00.html
43. sci-toys.com/ingredients/pectin.html
CIP – katlogizacija u publikaciji
Nacionalna i univerzitetska biblioteka Bosne i Hecegovine,Sarajevo (633/635:664.1/.9) (075.8)
JAŠIĆ, Midhat
Tehnologija voća i povrća. Dio 1, Opšte osobine i čuvanje, hemijski sastav, nutritivna svojstva, fizikalno – hemijska i senzorna svojstva
/ Midhat Jašić. -Tuzla : Tehnološki fakultet,
2007. – 369 str. : ilustr. ; 24 cm
Bibliografija uz svako poglavlje ; bibliografske i druge bilješke uz tekst
ISBN 978-9958-9456-9-4
COBISS . BH-ID 15933702