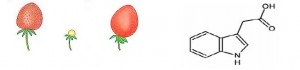Autor: prof. dr Midhat Jašić
Kontakt: midhat.jasic@untz.ba
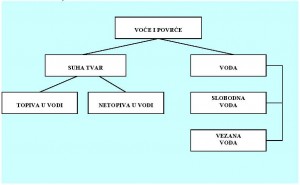
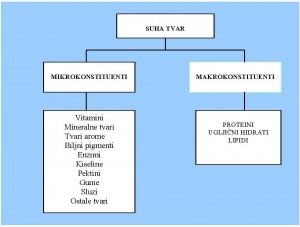
Osnovne komponente voća i povrća čine voda i suhe tvari. U sastav suhe tvari voća i povrća najčeće ulaze: ugljikohidrati, proteini (i ostale tvari sa N), lipidi, pektini, vitamini, mineralne tvari, voćne i mineralne kiseline, biljni pigmenti, taninske tvari, tvari arome, enzimi, prirodni premazi, sorbit, glukozidi i ostale tvari u tragovima. U pogledu hemijskog i nutritivnog sastava, voće i povrće sastoji se od:
Makrokonstituenata (voda, ugljikohidrati, proteini i lipidi) i
Mikrokonstituentata (vitamini, mineralne tvari, voćne i mineralne kiseline, biljni pigmenti, taninske tvari, tvari arome, enzimi itd).
Hemija voća i povrća proučava pojedine sastojke voća i povrća i promjene koje se s tim sastojcima događaju u prehrambenom lancu. Poznavanje hemijskog sastava je značajno sa tehnološkog aspekta kao i prepoznavanja i determiniranja primjerenih metoda konzerviranja. Hemijski sastav određuje prehrambena (nutritivna) svojstva, odnosno biološku vrijednost voća i povrća. Hemija voća i povrća obuhvata proučavanja sastava i promatranje hemijskih promjena u toku berbe, transporta, skladištenja, čuvanja, prerade i distribucije. Hemija voća i povrća proučava i uticaje prehrane na humani metabolizam kao i probavu voća i povrća. Nutricionizam pri tome uključuje i hemijske promjene i procese tokom humanog metabolizma voća i povrća. Očigledno je potrebno posebno poznavanje hemije voća i povrća na bazi: organske hemije (struktura i sistematizacija spojeva i procesa), fizikalne hemije (koloidi i fizikalna svojstva), biohemije (ciklusi i procesi) i analitičke hemije koja je potpora u dokazivanju konstituenata i kontroli tehnoloških procesa.
Topivost je prema hemijskim zakonima u funkciji temperature i pritiska. Tvari topive u vodi mogu biti: krute, tekuće igasovite. Topive krute tvari su: topivi proteini, amiloza, glukoza, fruktoza, saharoza, vitamini (B-kompleks, C vitamin), flavonoidi itd. U vodi topive tekuće tvar su naprimjer kiseline i alkoholi. Topive gasovite tvari: aromatske tvari (etri), CO2, H2, CH4, etilen (C2H2). U vodi nisu topive neke makromolekule koje se mogu nalaziti u voću i povrću, kao što je amilpektin iz škroba,celuloza i hemiceluloza, lignin, neke aminokisline i proteini, lipidi i sl.
Voda u voću i povrću
Voda je glavni sastojak voća i povrća sa značajnom funkcionalnom ulogom pošto neposredno učestvuje u izgradnji biljnih tkiva, a istovremeno ima utjecaja na odabir i primjenu metoda i postupaka konzerviranja. U odnosu na većinu namirnica povrće i voće je najbogatije vodom. Povrće općenito, sadrži 90-96% vode, dok voće normalno može sadržavati između 80 i 90%. Prisutna količina vode nalazi se vezana u raznim oblicima. Od načina vezanosti zavisi njena uloga u održavanju strukture kao i ponašanje i utjecaj na izvođenje tehnoloških postupaka prerade. Voda u voću i povrću može biti slobodna i vezana. S obzirom na mjesto gdje se nalazi u tkivu voda se može podijeliti na intracelularnu i ekstracelurarnu, odnosno na vodu koja se nalazi u ćelijama i vodu koja je smještena u međućelijskim prostorima. Prisutna je stalna razmjena vode između ćelije i njene okoline. Proces snabdijevanja ćelija hranljivim materijama obavlja se zahvaljujući tom procesu.Biljna stanica, općenito, sadrži znatne količine vode. U biljnoj stanici voda može biti vezana u slijedećim formama:
vezana voda u stanici (bound water /dilution water), a u njoj su rastvorene organske i mineralne tvari (vakuola)
- koloidno vezana voda koja se nalazi u membrani, citoplazmi i jezgri i koju je teže ukloniti tokom sušenja ili dehidratacionih procesa
- konstituciona voda je direktno vezana u hemijske komponente molekule koju je također vrlo teško ukloniti.
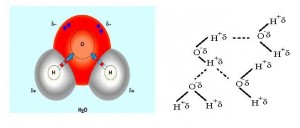
Molekula vode je polarna, negativan kraj jedne molekule privlači pozitivan kraj druge molekule. Zahvaljujući značajnom dipolnom momentu javlja se jaka interakcija zbog obrazovanja veza između atoma kisika jednog i atoma vodika drugog molekula. Ovo elektrostatičko vezivanje označava se kao vodikova veza. Voda je važna komponenta voca i povrca. Univerzalni je rastvarač soli , vitamina, secera , gasova , pigmentata i drugih konstituenata . Voda ima jonizaciona sposobnost :
2H2O ↔ H3O+ + OH–
Zbog svoje tekuće konzistencije na temperatureama iznad °C znantno ima uticaja na texturu voća i povrća. Voda stabilizira koloide hidratacijom. Takodje, učestvuje u biohemijskim reakcijama kao sto su hidroliza proteina do amino kiselina, hidrolizi skroba do sećera i sl . Omogućava rast mikroorganizama. Uslijed dipolnog karaktera oko molekule vode stvara se hidratni omotač. To se manifestira vezivanjem vode sa polarnim grupama, odnosno hidrofilnim radikalima kao što su hidroksil, amino, karboksil i slični radikali.
Većina najvažnijih makromolekularnih sastojaka voća i povrća ima hidrofilna svojstva, te vodu vezuje putem adsorpcije, gradeći pri tome hidrokoloide. Voda koja se na taj način adsorbuje naziva se hidratna voda. Ova količina vode proporcionalna je ravnotežnom sadržaju vode, a zavisi od energije vezivanja molekula vode sa odgovarajućim makromolekularnim sastojcima kao sto su želatin, škrob i sl. U raznim namirnicama za koje je karakteristična gel-struktura voda je „zarobljena“ tj. imobilizirana u potpunosti od strane prostorne konfiguracije stvorene od prisutnih suhih materija. Ovako se može objasniti kompaktan oblik i čvrsto stanje ljuštenog krastavca uprkos visokom sadržaju vode (skoro 95%), a također i mnogih drugih vrsta povrća sa 80-95%, odnosno mesa sa preko 70% vode.
Tabela 1. Približan sadržaj hidratne vode makromolekularnih komponenti
| Jedinjenje | Sadržaj hidratne vode(u % suhe materije) |
| Celuloza | 3-6 |
| Škrob | 7- 15 |
| Želatin | 15-25 |
| Pektin | 25-35 |
Mehaničko – fizikalno vezivanje vode. Tipično za ovu vrstu vezanosti vode u mnogim namirnicama je mogućnost njenog uklanjanja mehaničkim djelovanjima (na primjer presovanjem). Mehanički vezana voda pojavljuje se u više oblika i to kao: mikrokapilarna voda, makrokapilarna voda i površinaki vezana voda. Mikrokapilarna i makrokapilarna voda smještena je u kapilarama. Svojstveno za mikrokapilarnu vodu je činjenica da je tlak zasićene vodene pare u mikrokapilari manji nego što je u okolnom prostoru. To dovodi do kapilarne kondenzacije vode čak i u slučajevima kada je relativni sadržaj vlage okoline niži od 100%. Makrokapilarna voda se nalazi u kapilarama gdje je tlak zasićene vodene pare u kapilarama identičan sa tlakom zasićene vodene pare iznad ravne vodene površine. Površinaki vezana voda raspoređena je isključivo na spoljnim površinama. Ova voda je vezana čistom adhezijom, tj. nagomilavanjem na čvrstim česticama materija većih od pojedinačnih molekula. U odnosu na ostale načine vezivanja vode, ova veza je najslabija, tako da se voda može odstraniti bez teškoća, na primjer centrifugiranjem.
Slobodno ili vezano stanje vode u namirnicama od velikog je značaja i sa praktičnog stanovišta. Pod slobodnom vodom se podrazumijeva ona voda koja raspolaže punom sposobnošću rastvaranja. Adsorpciona voda je dijelom ograničena i u pogledu sposobnosti rastvaranja, a i u pogledu svoje pokretljivosti. Strukturalna voda, međutim, ima praktično istu sposobnost rastvaranja kao i slobodna voda, uprkos svoje prilične imobiliziranosti. Voda u mikrokapilarama, makrokapilarama, kao i površinski vezana voda, po svojim karakteristikama i aktivnosti spadaju u kategoriju slobodne vode.
Srazmjerno najviše slobodne vode sadrže tečne namirnice (voćni sokovi, kompoti, vino). Količinski je sadržaj vode u namirnicama sa mnogo masti mali, ali je sva ta količina ili „slobodna“ ili samo mehanički vezana. Najmanje slobodne vode imaju namirnice koje sadrže malo vode, a mnogo bjelančevina i ugljikohidrata (npr. sušeni proizvodi od povrća i voća, brašna, i sl.).
Sa biološkog stanovišta od praktičnog značaja je prvenstveno raspoloživa (slobodna) voda, a ne ukupna količina prisutne vode. Ravnotežni relativni sadržaj vode u prehrambenom proizvodu se označava pojmom hidrature. Vrijednost hidrature se može izraziti relativnim sadržajem pare (odnosno relativnim parnim tlakom) koji je u zatvorenom prostoru iznad namirnice u ravnoteži sa posmatranim proizvodom. Ravnotežni relativni sadržaj vlage pod datim uvjetima zavisi od količine raspoložive slobodne vode u dotičnoj namirnici. Ako je sva količina prisutne vode slobodna, odnosno stoji na raspolaganju, tada će vrijednost hidrature iznositi 100%. Vrijednost hidrature će opadati ispod 100 % srazmjerno povećanju količine vezane vode u namirnici.
U praksi se odnos parcijalnog tlaka vodene pare namirnice i tlaka čiste vodene pare na određenoj temperaturi definira kao aktivnost vode aw. Pomoću vrijednosti aw može se procijeniti koliki dio slobodne vode stoji na raspolaganju u odvijanju metabolizma prisutnih mikroorganizama. Izuzetna je važnost vlage sa mikrobiološkog aspekta pa je aw pogodan parametar pomoću kojeg se može kontrolirati rast i razvoj mikroorganizama. Utjecaj vrednosti aw je selektivan na aktivnost rasta mikroorganizama. Pored ovog utjecaja dokazan je i utjecaj vrijednosti aw na brzinu odvijanja raznih nepoželjnih hemijskih promjena u hrani, kao što su: autooksidacija (masti ), neenzimsko posmeđivanje, enzimska aktivnost, djelovanje plijesni, djelovanje kvasaca, aktivnost bakterija, itd. Za normalnu aktivnost bakterija potrebna najveća aw i to između 0.92 i 0.96. Za većinu kvasaca je neophodna vrijednost oko 0.88, za plijesni najmanje 0.75 – 0.80, za kserofilne plijesni oko 0.65. Najmanje potrebe u pogledu vode imaju osmofilni kvasci koji ne mogu živjeti u uvjetima u kojima je aw ispod vrijednosti 0.62. Na vrijednost aw utječu i faktori kao što su temperatura, pH sredine, sadržaj dodate soli i drugo. Komponente hemijskog sastava također imaju utjecaja na aw, naročito postojanje koloidne strukture.
Za aw usko je vezana higroskopnost, odnosno mogućnost upijanja i otpuštanja vodene pare iz okoline gdje je uskladišteno voće i povrće. Zavisnost između sadržaja vlage nekog proizvoda i relativnog sadržaja vlage okolne sredine u momentu uspostavljanja međusobne ravnoteže pri konstantnoj temperaturi prikazuju sorpcione izoterme.
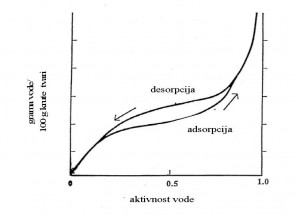
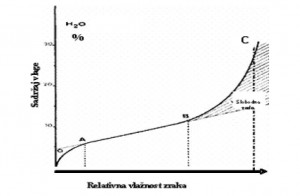
Grafički prikaz sorpcione izoterme se dobija povezivanjem niza tačaka izmjerenih sadržaja vlage namirnice kod uspostavljene ravnoteže sa okolinom poznate relativne vlažnosti (relativna vlažnost se mijenja, dok je temperatura konstantna). Konstruiranje sorpcionih izotermi može se vršiti praćenjem ovih korelacija.
Šematski prikaz sorbcione krive: do tačke A jako vezana voda, do tačke B umjereno vezana voda, do tačke C vodena otopina-slobdna voda.
Ako se polazi od suhog uzorka i prati postepeni prijem vlage uslijed kontakta sa okolinom veće relativne vlažnosti, tj. u slučaju većeg parcijalnog tlaka pare sredine od parcijalnog tlaka pare na površini uzorka, vlaga će se adsorbirati, a dobijena izoterma je adsorpciona izoterma. Vlažni proizvod će, u slučaju da se nalazi u dodiru sa sredinom male relativne vlažnosti, postepeno gubiti svoju vodu, tako da će se odigrati odgovarajuće sušenje. To se dešava uslijed postojanja većeg parcijalnog tlaka pare na površini namirnice od parcijalnog tlaka pare u okolini. Kriva dobijena povezivanjem ovako određenih ravnotežnih tačaka naziva se desorpciona izoterma. Razlika između toka adsorpcionih i desorpcionih izotermi naziva se histereza. U oba slučaja i kod prijema, i kod otpuštanja vode, prate se procesi do momenta uspostavljanja ravnotežnog stanja, tj. do izjednačavanja parcijalnih tlakova pare na površini namirnice i u okolnom vazduhu. Korištenjem elemenata sorpcionih izotermi formiraju se zaključci o ponašanju odgovarajućih namirnica, na osnovu kojih se mogu postaviti konkretni uvjeti sušenja, pakiranja i čuvanja.
Većina lisnatog povrća sadrži oko 90% vode (86% lisnati kelj, do 94% blitva). Slično je vodom bogato i cvjetasto povrće: brokula, prokulica i cvjetača od 86% (artičoka mladi cvjetovi) do 93% (listovi i cvijet cvjetače). Svježe mahunarke su bogate vodom. Sadrže 62% (mladi sirovi grah) do 90% (zelene mahune). Plodasto povrće (krastavci 96%, zelena paprika 94%, paradajz 98%) najbogatije je vodom od svih vrsta povrća. Stabljičasto (korabica, šparoge), gomoljasto povrće (krompir) i gljive također su bogati vodom (oko 80-93%). Voda se nalazi i u suhom povrću. U suhim mahunarkama (bob, grah, grašak, soja) ima oko 7-12% vode. U sojinu mlijeku vode ima 91%, a u tofu, sojinu siru, čak 85%. Svježe voće sadrži prosječno oko 80—90% vode. Najmanja vode je u bananama (71%), još manje u kruškama (oko 60%), a više u jabukama (87 %), trešnjama i višnjama (84%), dinjama i lubenicama (94%). Sušeno voće sadrži, svakako, mnogo manje vode, oko 10-20%. Iznimka su zelene, slane konzervirane masline sa 77% vode. U plodovima kestena ima oko 52%, u arašidu (kikiriki) i suhim, oljuštenim bademima nalazi se oko 4-7 % vode, u sirovom orahu 24%, a u suhom samo l% vode. U voćnim sokovima ima, što se i očekuje, dosta vode. Tako se u prirodnom svježem limunovom i narančinom soku nalazi 88% vode, a u soku rajčice čak 94% vode.
Makrokonstituenti suhe tvari voća i povrća
Suha tvar voća i povrća sastoji se iz mnogobrojnih vrsta hemijskih spojeva, najviše makromolekularnog tipa, kao što su: ugljikohidrati, a rjeđe masnoće i proteini. Hemijske biokomponente u svježem voću i povrću nalaze se u stanju vrlo dinamične biološke ravnoteže. Sadržaj suhe tvari je različit u različitim dijelovima tkiva biljke kao i u dijelovima biljne stanice.
Općenito suha tvar voća može se razlikovati po topivosti u vodi. Tako postoje u vodi topive tvari i netopive tvari .Topive tvari voća i povrća su uglavnom iz grupe koloida koji imaju veliku molekularnu težinu. Da bi se koloidno stanje ostvarilo, potreban je samo jedan uvjet: veličina čestica se mora kretati od 0.1 – 0.001 μ. To su najčešće pektini, škrob, dekstrini, bjelančevine, neki tanini i dr. Karakteristično je da su to elektroliti i nose pozitivan ili negativan električni naboj. Koloidi se nalaze u sol ili gel stanju. SOL je disperzija čvrstih čestica u tekućini. Ove čestice mogu biti makromolekule ili nakupine malih molekula, a mogu biti i: liofilni ili liofobni. Liofobni solovi su takvi solovi kod kojih ne postoji afinitet između dispergirane faze i tekućine (vode hidrofobni). Oni su po prirodi nestabilni, vremenom koaguliraju i istalože se. Liofilni solovi su mnogo sličniji pravim otopinama. Stabilni su i teško se koaguliraju (npr. škrob u vodi).GEL je koagulirani oblik koloidnih sistema u kojem obje fazi prave trodimenzijsku mrežu kroz materijal (nprimjer želatin ).
Koloidi imaju sposobnost stvaranja micela, električno nabijenih čestica sastavljenih od nakupina velikih molekula. U vodenim otopinama hidrofilni krajevi ovakvih molekula su na površini micele, dok se hidrofobni kraj (obično ugljikovodikov lanac) usmjerava prema središtu. Koloidni ioni nastaju kada koloidne čestice adsorbiraju određenu vrstu iona iz otopine i nabiju se istovrsnim nabojem. Naboj može potjecati i od hemijske reakcije površine čestice. Imaju sposobnost hidratacije. Odnos između koloidnih čestica i medija – vode u kojem su otopljene obično ima hidrofilni status (hidrokoloidi). Općenito koloidi mogu biti u formi:
- suspenzije,
- emulzije,emulzije
- disperzije.
Suspenzije su u formi sitnodispergiranih čestica unutar otopine i nalaze se u krutom stanju. Nakon nekog vremena se talože. Podjednako su raspoređene u rastvoru zahvaljujući stabilizatoru. Kod emulzija dispergirano stanje čestica održavaju emulgatori. Disperzija ovisi o električnom naboju i zakonitostima Brownovog kretanja.
Tabela 2. Orjentacioni sastav suhe tvari voća i povrća
| Naziv konstituet | % | Komentar |
| Ugljikohidrati | 3 – 18 % | Ovisi o vrsti i sorti |
| Sirova vlakna | 0.3 – 6,0% | Kod nekih vrsta povrća i voća i više |
| Tvari sa nitrogenom | 0.8 – 1,3% | Kod orašastog voća i leguminoza i više |
| Mineralne tvari | 0.3 – 0,8% | Kod nekih vrsta povrćai voća i više |
| Masti | 0.1 – 0.3% | Kod orašastog voća i leguminoza puno više |
Osim makromolekularnih spojeva u suhu tvar ulaze i kristaloidi, koji imaju manju molekularnu težinu i manji su po veličini čestica. Kristaloidi su substance po molekulskoj masi manje od koloida, u otopinama prolaze kroz semmipermeabilne membrane, snizuju tačku mržnjenja otopine i općenito imaju sposobnost kristalzacije. To su: šećeri, kiseline i neke mineralne tvari, koji u vodi prave prave otopine.
Ugljični hidrati
Ugljični hidrati su hemijski konstituenti hrane koji imaju važnu energetsku ulogu u biološkom sistemu hrane. Mogu se pojavitiu voću i povrću kao njihovi makrokonstituent ili mikrokonstituenti. Validiraju se kao energetske i biološki aktivne komponente hrane. Sa energetskog aspekta, ugljikohidrati predstavljaju najviše validiranu komponentu u hrani. Ugljični hidrati su proizvodi oksidacije polivalentnih alkohola, odnosno oni su aldehidi ili ketoni alkohola ili jedinjenja nastala kondenzacijom polivalentnih alkohola. Jednostavno, ugljični hidrati su spojevi ugljika-karbonilni spojevi, sastavljeni od jedne ili više jedinica poli-hidroksi-aldehida ili ketona. Ugljični hidrati koji sadrže aldehidnu grupu nazivaju se aldoze, a ugljični hidrati koji sadrže keto grupu ketoze. U romanskim jezicima nazivaju ih glicidi (franc, glucides, tal. glicidi. Često se upotrebljava i naziv saharidi (prema lat. saccharum = šećer).Ugljični hidrati se dijele na tri velike grupe: jednostavne šećere, oligosaharide i polisaharide.
Tabela 3. Podjela ugljikohidrata
| Grupa | Stepen polimerizacije | Podgrpa | Komponente u prehrani |
| Jednostavni šećeri | 1 do 2 | Monosaharidi | Glukoza,galaktoza fruktoza |
| Polioli | Sorbitol, manitol | ||
| Oligosaharidi | 2 | Disaharidi | Saharoza, laktoza,Maltoza, trehloza |
| 3 do 9 | Malto-oligosahridi | Maltodekstrini,rafinoza stahioza | |
| Polisaharide | Veći od 9 | Skrob | Amiloza, amilopektin, modificirani skrob |
| Neskrobni polisaharidi | Celuloza Hemiceluloza, Pektini, Sluzi, gume |
Ugljični hidrati nastaju procesom fotosinteze. Stvaraju se u zelenim biljkama asimiliranjem ugljik-dioksida (CO2) i vode uz fotosintezu iskorištavanjem Sunceve energije. Oni su strukturalne komponente u slučaju celuloze, sačinjavaju energetske rezerve u slučaju biljnih škrobova, imaju esencijalne funkcije kao komponente nukleinskih kiselina u slučaju riboze i kao komponente vitamina u slučaju riboze i riboflavina.Ugljikohidrati oksidacijom oslobadjaju energiju. Glukoza je u krvi čovjeka primarni izvor energije za ljudsko tijelo. Fermentacijom ugljikohidrata pomoću kvasaca i drugih mikoorganizama može se proizvesti ugljen dioksid, alkohol, organske kiseline i druge komponente.
Šećeri. Šećeri sačinjavaju najveći dio rastvorljivih suhih materija koji se određuju kao refraktometrijska vrijednost. Zajedno sa kiselinama oni prestavljaju osnovnu komponentu u formiranju ukusa proizvoda. Sadržaj ukupnih šećera varira u dosta širokim granicama, što zavisi od vrste, sorte, stepena zrelosti, kao i od uslova gajenja. Jagodičasto voće može da sadrži od 2.5 do 15 % šećera, koštičavo voće od 3 do 15 %, a jabučasto od 6 do 17 % . Od povrća šećerom su bogati mrkva, kupus, crni luk, crveni patlidžan, grašak i paprika. Međutim, taj sadržaj je znatno manji u odnosu na sadržaj šećera u voću. Tako kupus može da ima šećera od 1.4 do 5 %, crveni patlidžan 1.5 do 3 % , grašak od 2 do 6 %, crni luk od 2 do 5 %, mrkva oko 5.5 % i karfiol oko 3 %. Šećeri mogu biti reducirajući i nereducirajući. Reducirajući šećeri imaju slobodnu aldehidnu skupinu ( reducens) ili keto-skupinu koja može izomerizirati u slobodni aldehid. Kod polisaharida razlikujemo reducirajuće i nereducirajuće krajeve lanaca, ovisno o tome može li se prsten monosaharidne jedinice na kraju lanca otvoriti u slobodnu aldehidnu skupinu. Svi nemodificirani monosaharidi su reducirajući. Saharoza je primjer nereducirajućeg disaharida. Kod saharoze glikozidna veza spaja dva anomerna ugljika (C1 glukoze i C2 fruktoze) te nije moguće otvaranje niti jednog od dvaju prstenova.
Monosaharidi i disahardi. Monosaharidi (grč. monos = sam, jedan) su najjednostavniji ili osnovni saharidi koji se, osim pri stvaranju energije u organizmu, ne mogu cijepati na manje molekule. Sadrže 3-7 atoma ugljika.
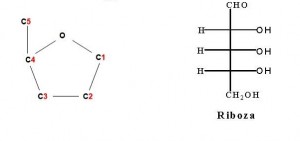
Dijelimo ih na pentoze i heksoze. Pentoze sadrže pet atoma ugljika i pet molekula vode (C5H10O5). Važnije pentoze su arabinoza i ksiloza, dok je riboza sastavni dio nukleinskih kiselina i koenzima koji se nalaze u svim stanicama, ali u vrlo malim razmjerima. Postoje još liksoza, dvije ketoze, ribuloza i ksiluloza, koje se pojavljuju samo u biosintezi. Arabinoza se nalazi u slobodnom obliku, ali u relativno malim količinama u nekim vrstama voća i gomolja odnosno lukovica, npr. u šljivi, višnji, luku. Ljudski je organizam ne može metabolizirati. Ksiloza se u manjim količinama nalazi slobodna u nekim vrstama voća (npr. u marelici), a ljudski organizam je ne može metabolizirati.
Heksoze su najvažniji i u prirodi najrašireniji šećeri. Nalaze se kao slobodni ili kao vezani spojevi. To su glukoza, galaktoza i fruktoza, te za prehranu manje važne manoza, ramnoza i sorboza.
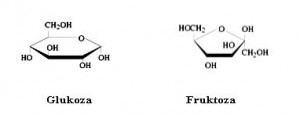
Glukoza (C6H12O6) je grožđani šećer, obilno prisutna u voću. Osnovni je izvor ugljikohidratne energije. Glukoza predstavlja nesumnjivo najvažniji šećer za živu stanicu ogromne većine organizama. Ona čini najveći dio ugljikohidrata koji se koristi u ishrani čovjeka, domaćih životinja, kao i u metabolizmu biljaka.
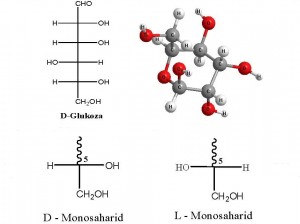
Fischerovom projekcijskom formulom, vidimo da glukoza ima četiri kiralna centra C-2, C-3, C-4 i C-5. Svi monosaharidi kod kojih je hidroksilna skupina na kiralnom atomu ugljika (koji je označen najvećim brojem, u ovom slučaju C-5) smještena na desnoj strani se nazivaju D-monosaharidi, a ako je OH skupina na lijevoj strani onda su to L-monosaharidi.
L-šećeri su manje rasprostranjeni u prirodi u odnosu na D oblike, ali ipak imaju važnu biološku ulogu.
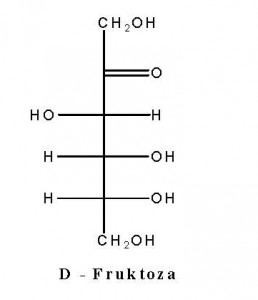
Fruktoza (lat. fructus = plod, ljetina) je voćni šećer, a nalazi se i u mnogim vrstama povrća U medu su, na primjer, podjednake količine fruktoze i glukoze.
U spoju s drugim supstancama fruktoza se krije u velikom broju oligosaharida (saharozi, rafinozi, inulinu i drugima).Fruktoza je izomerni šećer glukoze, i svrstava se u ketoheksoze. D-fruktoza ima samo tri kiralna atoma ugljika C-3, C-4 i C-5. Fruktoza je najznačajnija ketoza. U ljudski organizam dospijeva kroz hranu. To je prirodni šećer kojeg osim u voću, povrću i medu, ima i u u visokofruktoznom šećeru (proizvod dobijen hidrolizom skroba iz kukuruza). To je izomer glukoze. Hidrolizom saharoze u organizmu nastaju glukoza i fruktoza. Fruktoza se kao i glukoza direktno apsorbuje u krv. Krv je odnosi u jetru gdje dolazi do izomerizacije fruktoze u glukozu, koja se kasnije u ćelijama koristi za stvaranje energije.
Za razliku od saharoze, fruktoza je puno slađa i lakše se topi u vodi. Kako je fruktoza lijevo okrenuta ketoheksoza zovu je, osobito u farmakologiji, levuloza. Iz crijeva se resorbira brže nego glukoza.
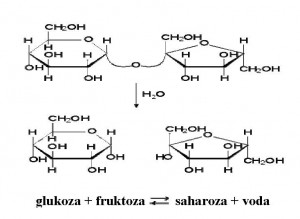
Disaharidi su šećeri sastavljeni od dvije molekule monosaharida spojene glikozidnom vezom. Oni nastaju međusobnim povezivanjem dviju jednakih ili različitih molekula monosaharida uz gubitak jedne molekule vode. Tako, primjerice, saharoza (C12H22O11) nastaje međusobnim povezivanjem jedne molekule glukoze (C6H12O6) i jedne molekule fruktoze (C6H12O6). Djelovanjem vode uz prisutnost kiseline ili nekog enzima disaharidi se razlažu na monosaharide od kojih su nastali. Među najraširenije disaharide ubrajamo: saharozu, laktozu, maltozu i celobiozu. Saharoza (poznata kao šećer ) je glukoza + fruktoza. Saharoze najviše ima u šećernoj repi (16-20 %) i u šećernoj trsci (14-26%), pa je zbog toga još dobila ime tršćani ili repin šećer. To je bijela supstanca koja kristališe u vidu sitnih bezbojnih kristala, vrlo slatkog okusa. Ona se hidrolizom raspada na glukozu i fruktozu. Hidroliza se vrši u prisustvu katalizatora, kiseline ili enzima invertaze. Hidrolizom saharoze nastaje invertni šećer. Invertni šećer je ekvimolarna smijesa glukoze i fruktoze i javlja u obliku sirupa.
Tabela 4. Stupanj slatkoće različitih prirodnih hemijskih spojeva
| Tvar | Relativna slatkoća |
| Šećeri | |
| Ksiloza | 0,7 |
| Glukoza | 0,5 – 0,8 |
| Fruktoza | 1,2 – 1,5 |
| Galaktoza | 0,6 |
| Manoza | 0,4 |
| Laktoza | 0,2 |
| Maltoza | 0,5 |
| Saharoza | 1,0 |
| Polioli | |
| Manitol | 0,6 |
| Laktitol | 0,3 |
| Izomaltitolc | 0,4 – 0,6 |
| Ksilitol | 1,0 |
| Sorbitol | 0,5 |
| Maltitol | 0,8 |
| Hidrogenirani kukuruzni sirup | 0,3 – 0,75 |
Laktoza – mliječni šećer je glukoza + galaktoza, nalazi se u mlijeku svih sisara, a dobija se kao sporedni proizvod kod proizvodnje sira. To je redukujući disaharid, koji kiselom ili enzimatskom hidrolizom daje glukozu i galaktozu. Empirijska formula je C12H22O11.Nije zastupjena u voću i povrću.
Maltoza je produkt koji nastaje tokom proizvodnje slada. Biohemijski se sintetiše međusobnim povezivanjem dvije molekule glukoze, gdje su monomeri glukoze povezani sa α(1→4) vezama. Maltoza, C12H22O11 nastaje iz škroba dijelovanjem fermenta dijastaze. Hidrolizom maltoze u kiseloj sredini nastaje D-glukoza.
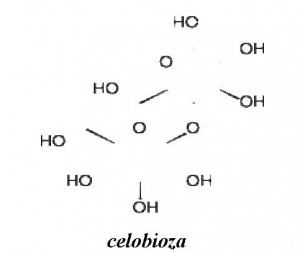
Trehaloza je prisutna kod gljiva i insekata. Takođe nastaje međusobnim povezivanjem dvije molekule glukoze, gdje su monomeri glukoze povezani sa α(1→1) vezama. Celobioza je još jedna glukoza + glukoza disaharid, gdje su monomeri glukoze povezani sa β(1→4) vezama. Nastaje djelomičnim cijepanjem celuloze. Nema većeg praktičnog značenja za ljudski organizam.
Trisaharidi i tetrasaharidi . To su oligosaharidi s tri odnosno četiri molekule monosaharida. Od praktične je važnosti rafinoza koja se nalazi u melasi (međuproizvod pri proizvodnji šećera) šećerne repe kao i stahioza u sojinom mlijeku.
Rafinoza je trisaharid koji je sastavljen od galaktoze, glukoze i fruktoze. Stahioza se sastoji od dvije molekule galaktoze, jedne molekule glukoze i jedne molekule fruktoze. Voće i povrće koje sadrže stahiozu, rafinozu, verbaskozu u debelom crijevu podliježu bakterijskom razlaganju uz stvaranje plinova (vodik, metan). To su: šljive, grah, soja, rotkvica, luk. Za ove polisaharide u crijevima ne postoje adekvatni enzimi zbog čega stvaraju plinove.
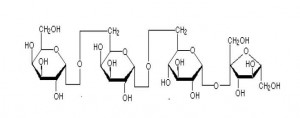
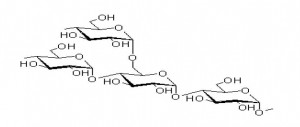
Polisaharidi. Polisaharidi (grč. polys = mnogi) se sastoje od deset i više molekula monosaharida i nastaju njihovim udruživanjem u visokomolekulski spoj, uz odvajanje vode. Važniji polisaharidi su: homoglikani i heteroglikani. Među homoglikane ubrajamo: škrob, glikogen i celulozu, a među heteroglikane: mukopolisaharide, gume i pektine. Od velikog praktičnog značenja su škrob i celuloza, ali i rezervni biljni polisaharid inulin. Svi spomenuti spojevi služe kao rezerve ugljikohidratne energije (škrob) ili izgraduju čvrste stanične strukture, tvoreći »kostur« stanice (celuloza).
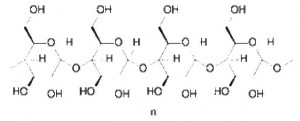
Škrob. Stvara se u zelenim dijelovima biljaka kao primarni proizvod fotosinteze. Najviše ga ima u krompiru i žitaricama. Najvažnija je ugljikohidratna hrana čovjeka. Velika se molekula škroba sastoji od glukoznih ostataka. Zrnca škroba sastoje se od dviju frakcija različite građe: amiloze (oko 10-20%) i amilopektina (80-90%). Amiloza je linearni polimer glukoze. Može biti napravljen od nekoliko hiljada glukoznih jedinica. Celuloza i amiloza, pripadaju grupi polisaharida sa jednoličnim lancima.
Amilopektin je visoko rangiran polimer glukoze nađen u biljkama. Amilopektin pripada polisaharidima s razgranatim lancima. U biljkama nastaje u specijalnim organelama zvanim amiloplasti. Ljudi i ostale životinje koji jedu biljnu hranu imaju enzime za hidrolizu amilopektina.
Amiloza se nalazi u šrobnom zrncu, a amilopektin u njegovu površinskom sloju. Dekstrini su međuproizvodi koji se stvaraju pri enzimskoj ili pri kiseloj razgradnji škroba na sobnoj temperaturi. Neke važnije osobine škroba su:
- predstavlja rezerve energije u biljkama i snabdijeva energijom ljudsko tijelo tokom prehrane
- stvara u sjemenu i krtolama karakteristične škrobne granule.
Prema porijeklu razlikuje se škrob pšenice, riže, krompira, kukuruza i drugih biljaka. U biljkama se deponuje u plodovima, korijenu i služi kao rezervna hrana. Tako je npr. škrob u bananama vrlo otporan na probavnu razgradnju, pa je i brašno pripravljeno od banana i krompira jako otporno na probavu.
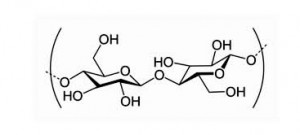
Celuloza. Celuloza i hemiceluloza spadaju u pentozane (sirova vlakna).Celuloza je kvantitativno najzastupljeniji ugljikohidrat u prirodi. Nalazi se isključivo u biljkama, čini građu celularnog »kostura«. Glavni je sastojak staničnih membrana biljaki, a nalazi se i u kori, sjemenkama i sl. Ljudski organizam ne može iskoristiti celulozu jer nema enzima celulazu, koja je razgrađuje. Svi biljožderi imaju celulazu, pa je za njih celuloza važan izvor ugljikohidratne hrane. Bakterije prisutne u debelom crijevu čovjeka imaju značajnu ulogu u konačnoj razgradnji neprobavljenih ostataka hrane, ali tek neznatnu ulogu u razgradnji celuloze u ljudskom kolonu. Celuloza je vrlo stabilan ugljikohidrat, netopiv u vodi. Ipak zadržava (apsorbuje) vodu, tvori glavnu masu neprobavljene hrane, pospješuje pražnjenje crijeva. Povoljno djeluje i na dijabetične bolesnike, omogućavajući posredno bolju utilizaciju ugljikohidrata. Neke važnije osobine celuloze i hemiceluloze su:
- primarno čine strukturu i održavaju konfiguraciju biljnih listova i zelenih dijelova biljke,
- nerastvorljivi su u toploj i hladnoj vodi,
- nisu probavljivi u ljudskom organizmu i ne daju energetski prinos u njemu i
- to su tzv. biljna vlakna i imaju funkciju u stvaranju balasta u organizmu.
Celuloza se sastoji od jedinica glukoze međusobno povezanih hemijskim vezama. Jedna molekula celuloze može imati čak do 10 000 jedinica glukoze. Celuloza zato ima izgled finih tankih niti. Hemijski je vrlo slabo reaktivna, što je posljedica njezinih fizikalnih svojstava. Celuloze najviše ima u mekinjama pšeničnog brašna, u punozrnatim žitaricama, u koži voća i povrća.
Hemiceluloza je također sastavljena od mnogih jedinica heksoza, pentoza i uronskih kiselina. Hemiceluloza je polimer glukoze i drugih heksoza, pentoza i uronskih kiselina koje se nalaze u stijenkama gotovo svake biljne stanice. Ipak joj je lanac mnogo kraći pa obično nema više od 20 do najviše 2000 jedinica.
Inulin nastaje polimerizacijom fruktoze, pa ga nalazimo samo u biljkama (cikorija, gomolji mnogih biljaka, od kojih su mnoge ljekovite). Sadrži oko 30 molekula fruktoze (fruktoznih ostataka). Ljudski ga organizam ne može upotrijebiti kao hranu jer nema za to potrebnih enzima, pa ga nepromijenjena izlučuje putem bubrega.
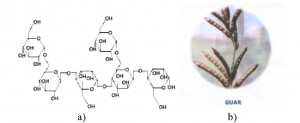
Gume (karbohidratni spojevi) imaju osnovnu funkciju održanja konzistencije biljnog tkiva. To su u vodi topivi viskozni, gusti polisaharidi. Sadrže 10 000 do čak 30 000 jedinica i to glukozu, galaktozu, manozu, arabinozu, ramnozu i njihove uronske kiseline. Industrija hrane ekstrahira ih iz prirodnih izvora. To su arapska guma koju stvara stablo jedne akacije Robinia pseudoacacia, zatim tragakant guma iz nekih vrsta stabala, guar guma koja se dobiva iz jedne indijske mahunarke i guma iz dalmatinskoga rogača. Iz njih se prave emulzije, stabiliziraju razne namirnice i zgušnjavaju sirovine pri industrijskoj obradi raznih vrsta hrane. Razlikujemo gume koje se stvaraju na stablima i gume koje se mogu ekstrahirati iz brašna. Od guma koje se dobivaju iz zdrobljenih zrnaca poznatija je guma guar indijske biljke (Cyamopsis tetragonolobus). Kristalna koloidna struktura karakteriše prah koji se dobija iz guar gume koja se danas upotrebljavaju u prehrambenoj industriji kao hidrokoloid.
Sluzi su također polimeri ugljikohidrata. Prirodni im je izvor sjemenje i korijenje, u kojima se služi biljkama kao sredstvo koje sprječava isušivanje. Najviše ih prirodno ima u algama i morskoj travi. Prehrambena industrija koristi ih kao stabilizatore i uguščivaće u raznim jelima.Sluzi su prirodni, biljni heteropolisaharidi i predstavljaju rezerve ugljenih hidrata i vode u biljci. Izgradjeni su od linearnih ili račvastih lanaca : pentoza, heksoza i uronskih kiselina, njihovih soli i estara.
Sluzi sa linearnim nizovima grade vodene rastvore velike viskoznosti i male stabilnosti (pri promjeni temperature dolazi do kidanja vodenih veza i do njihovog taloženja). Sluzi sa račvastim lancima polisaharida sa vodom formiraju gelove, stabilne sisteme.
Sluzi su u najvećoj koliičini koncetrisane u biljkama kiao :kisele sluzi i neutralne sluzi. Lokalizovane su u raznim delovima biljaka u obliku membranske sluzi (nagomilane na ćelijskim zidovima), sekundarnih zadebljanja ili ćelijske sluzi (bezoblične mase u ćeliji).
Proteini i ostale tvari s dušikom
Ove supstance se nalaze u biljci u različitim kombinacijama, tj. kao sastavni dio proteina, aminokiselina, amida, amina i nitrita. Povrće ih sadrži izmedju 1.0 i 5.5 % dok ga voće sadrži u količinama ispod 1% u većini slučajeva. Od tvari s dušikom najvažniji su proteini, koji imaju koloidnu strukturu. Naziv protein potiče od grčke riječi proteos, sto znaci prvi ili najvaznij. Protein je kompleksan organski spoj, visoke molekularne težine koji se sastoji od aminokiselina povezanih peptidnom vezom i karakterišu ih veoma krupni molekuli. Proteini mogu biti rastvorljivi ili nerastvorljivi u vodi. U građi molekula proteina su zastupljeni kiseonik, vodonik, ugljenik i azot, a u nekim i sumpor ili fosfor. Ovi elementi ulaze u sastav amino-kiselina. Amino-kiselinski sastav proteina nije isti i predstavlja najvažniju karakteristiku svakog proteina, a služi i kao kriterijum odredjivanja biološke vrijednosti u prehrani. Broj amino-kiselina koje mogu da ulaze u sastav proteina je 20-22. One svojim različitim kombinovanjem obrazuju izvanredno veliki broj različitih proteina. Neke od njih čovjekov organizam može sam da sintetizuje, dok neke ne može. Esencijalne (nezamjenjive) aminokiseline moraju se unositi u organizam kroz hranu.
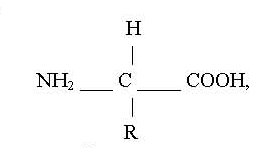
Aminokiselina je organski spoj koji sadrži i amino (-NH2) i karboksilnu (-COOH) skupinu. R je aminokiselinski ogranak (slobodni radikal). Kod glicina je to H atom. Aminokiselinski ogranci kod ostalih aminokiselina su: alifatski ( alanin, valin, leuci, izoleucin), imino skupina (prolin), alifatska hidroksilna skupina ( serin i treonin), aromatske skupine (fenilalanin, tirozin, triptofan), bazne skupine ( lizin, arginin, histidin), kiseli ogranci ( aspartat i glutamat), amidni ogranci ( asparagin i glutamin) i ogranci sa sumporom ( cistin i metionin).
Aminokiseline mogu i ne moraju biti topljive u vodi to ovisi o slobodnom radikalu(R). One su optički aktivni spojevi (svi osim glicina) što znači da mogu zakretati ravninu polarizirane svjetlosti i sadrže bar jedan asimetričan C-atom( L i D izomeri ). Proteini su izgrađeni samo od L-aminokiselina. Aminokiseline su amfoterni spojevi – to znači da se mogu ponašati kao kiseline i kao baze, ovisno o pH medija u kojoj se nalaze.
Tabela 5. Aminokiseline neophodne za gradnju proteina u ljudskom organizmu
| Esencijalne (nezamjenjive )aminokiseline | ||
| Izoleucin | Lizin | Treonin |
| Leucin | Metionin | Triptofan |
| Fenilalanin | Valin | |
| Semiesencijalne aminokiseline | ||
| Arginin | ||
| Histidin | ||
| Neesencijalne (zamjenjive )aminokiseline | ||
| Alanin | Cistein | Prolin |
| Asparagin | Glutaminska kiselina | Serin |
| Asparaginska kiselina | Glutamin | Tirozin |
| Glicin | 1 | |
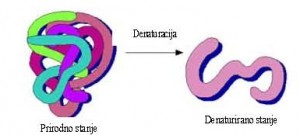
Spajanjem aminokiselina u dugačke lance nastaju proteini, čija se molekulska masa kreće od 30000 do nekoliko stotina hiljada. Posjeduju sinergičnost jer zajedno sa mastima (fosfolipidima) grade sve biološke membrane. Termičkom obradom, tretiranjem bazama i kiselinama, sušenjem, soljenjenjem, zračenjem dolazi do njihove denaturizacije. Pod uticajem različitih faktora (kiseline, baze, promjena pH, visoke temperature i sl) trodimenzionalna struktura proteina se može narušiti pri čemu dolazi do odmotavanja lanaca.Ta promjena se naziva denaturacijom proteina.
U odnosu na porijeklo, proteine dijelimo na biljne i životinjske. Prema sastavu proteini se dijele na: proste proteine ili proteine u užem smislu i složene proteine ili proteide. Prosti proteini biljnog porijekla su: prolamini i glutelmini, a životinjskog albumini, globulini, protamini, histoni, skleroproteini.
Tabela 6. Podjela proteina prema složenosti
| Prosti proteini | Složeni proteini |
| a) Pravi proteini | Hromoproteidi |
| Protaminihistoni | Nukleoproteidi |
| Globulini | Glukoproteidi |
| Prolamini | Fosfoproteidi |
| Albumini, | Lipoproteidi |
| Glutelin | |
| b) Skeletni proteini: | |
| Keratini | |
| kolagen |
Prosti proteini se hidrolizom razlažu do aminokiselina, a složeni proteini pored aminokiselina hidrolizom daju i druge materije (ugljikohidrate, nukleinske kiseline, fosfor i sl). Proteidi, koje u svom sastavu imaju, osim amino-kiselina i nebjelančevinastu komponentu. To je nekad mast, šećer, nukleinska kiselina ili specifična bojena materija. Prema prirodi te komponente, proteine možemo podijeliti na gradivne i biološki aktivne. Složeni proteini su:
- metaloproteini (prostatska skupina i metal: transferin, ceruloplazmin)
- lipoproteini (lipid + protein: HDL, LDL, VLDL)
- glikoproteini (šećer + protein)
- nukleoprotein (nukleinska kis + protein)
- fosfoproteini (fosfor + protein)
- kromoproteini (u boji – hemoglobin)
Gradivni proteini , zajedno sa drugim organskim makromolekulima, ulaze u građu protoplazme, dok drugi učestvuju u regulaciji metaboličkih procesa i ostalih funkcija živih bića. Sa biološkog – nutritivnog aspekta biljni proteini su manje vrijedni od životinjskih i njihova kompozicija ne sadrži većinu esencijalnih aminokiselina. Izvori biljnih proteina su : orasi, proklijala zrna, sjemenke, grah, grašak, soja , pečurke i drugo voće i povrće. Najbogatije proteinima je jezgrasto voće (orasi 15 – 20%; bademi 22 -35%) dok jagodasto sadrži 0.1 – 0.33 %, a koštuničavo 0.07 – 0.21 %. Najsiromašnije je jabučasto voće 0.03 – 0.13%.
Lipidi – masnoće
Općenito, voće i povrće sadrži vrlo malo masnoća, ispod 0.5%. Međutim, značajne količine naleze se u orasima (55%), sjemenu kajsije (40%), sjemenu grožđa (16%), sjemenu jabuke (20%) i sjemenu paradjza (18%). Značajnija ulja koja imaju primjenu u prehrambenoj industriji, a dobijaju se iz voća i povrća su: bademovo, ulje kajsije, avokada, kakaoa, arašida,bundeve i soje.
Lipidi su jedinjenja različitog sastava po pravilu nerastvorna u vodi, a rastvorna u organskim rastvaračima. Osnovna su komponenta bioloških membrana i utiču na njihovu propustljivost, učestvuju u predaju nervih impulsa, stvaraju kontakte među ćelijama, čine energetske rezerve, štite organizam od mehaničkih povreda i formiraju termoizolacionu sloj. Lipid obuhvataju širok spektar molekula raznovrsne hemijske strukture biološkog porijekla ukljućujući :
- masti i ulja
- voskove ,
- masne kiseline i izvedene fosvolipide,
- sfingolipide,
- glikolipide i
- terpenoide kao što su retinoidi i steroidi.
U svim zivim ćelijama javljaju se kao strukturna komponenta. Neki lipidi su linearne alifatske molekule, dok drugi imaju prstenastu – ring strukturu. Neki su aromatski, dok drugi nisu. Neki lipidi imaju izvjesni polarni karakter dok su drugi nepolarni. Općenito, njihova izvorna struktura je nepolarna ili hidrofobna što znači da ne postoji dobra intereakcija sa polarnim otapalima kao što je voda. Neke grupe lipida mogu imati dio strukture koji je polaran ili hidrofilni i pokazuje dobru tendenciju da se združe sa polarnim otapalom kao što je voda. Općenito ova pojava ih čini amfilitnim molekulama (posjeduju oba svojstva hidrofilno i hidrofobno ). U slučaju kolesterola to je -OH (hidroxil ili alkohol). U slučaju fosvolipida polarne grupe su veće i više polarizirane.
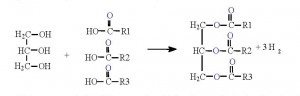
Molekul masti se sastoji od tri molekula masnih kiselina, koje su vezane za jedan molekul trihidroksilnog alkohola glicerola. Masti koje sadrže nezasićene masne kiseline (sa dvostrukim vezama izmedju ugljenikovih atoma) zapravo su ulja, karakteristicnija za biljke nego za zivotinje. Molekuli masti kao izvor energije deponuju se u masnim (adipoznim) celijama, koje sadrze mnoge lipidne kapljice.
U sastav masti ulaze masne kiseline sa 4-26 ugljenikovih atoma i to samo masne kiseline sa parnim brojem C atoma. U sastavu većine masti dominiraju masne kiseline sa 16-18 atoma ugljenika u lancu (palmitinska, stearinska i oleinska).
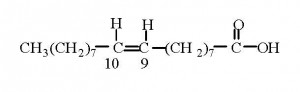
Zavisno od broja vodonikovih atoma koji su vezani na slobodne valencije ugljenika u molekuli kiseline razlikuju se tri tipa masnih kiselina: zasićene, mononezasićene i polinezasićene. Na svim atomina ugljenika kod zasićenih masnih kiselina vezanje maksimalan broj atoma vodonika, odnosno svi ugljenikovi atomi su „zasićeni“ vodonikom. Ovaj tip masnih kiselina dominira u mastima koje su čvrste na sobnoj temperaturi (masti životinjskog porijekla). Mononezasićene masne kiseline imaju takav hemijski sastav koji im omogućuje vezivanje još dva atoma vodika u molekuli masne kiseline. Masti u čijem su sastavu prisutne takve masne kiseline nalaze se u tekućem agregatnom stanju pri sobnoj temperaturi. Te su namirnice redovito biljnog porijekla i nazivamo ih biljnim uljima. Najrasprostranjenija masna kiselina koja spada u porodicu mononezasićenih masnih kiselina je oleinska kiselina, glavni sastojak maslinovog ulja.
Polinezasićene masne kiseline imaju više „slobodnih“ mjesta na atomima ugljika na koje mogu vezati atome vodika. Najpoznatija od tih masnih kiselina je linolna masna kiselina koja ulazi u sastav brojnih biljnih ulja poput suncokretovog, kukuruznog i sezamovog. Veliki izvor polinezasićenih masnih kiselina su ribe, a naročito plava riba.
Tabela 7. Najčešće masne kiseline
| Zasićene masne kiseline | ||
| 12:0 | Laurinska | CH3(CH2)10COOH |
| 14:0 | Miristinska | CH3 (CH2)12COOH |
| 16:0 | Palmitinska | CH3 (CH2)14COOH |
| 18:0 | Stearinska | CH3 (CH2)16COOH |
| 20:0 | Arašidna | CH3 (CH2)18COOH |
| Nezasićene masne kiseline | ||
| 16:1 | Palmitoleinska | CH3 (CH2) 5CH=CH(CH2) 7COOH |
| 18:1 | Oleinska | CH3 (CH2) 7CH=CH(CH2) 7COOH |
| 18:2 | Linolna | CH3 (CH2) 4 (CH=CHCH2) 2 (CH2)6COOH |
| 18:3 | Linolenska | CH3CH2 (CH=CHCH2) 3 (CH2) 6COOH |
| 18:3 | Linoleinska | CH3 (CH2) 4 (CH=CHCH2) 3 (CH2) 3COO |
| 20:4 | Arahidonska | CH3 (CH2)4 (CH=CHCH2)4(CH2 )2COOH |
Esencijalne masne kiseline Masne kiseline sa više dvostrukih veza (linolna, linolenska i arahidonska) ubrajaju se u esencijalne sastojke hrane, jer se ne mogu sintetizovati u organizmu. Linolna kiselina ima prvu dvostruku vezu između 6. i 7. ugljenikova atoma, zbog čega se naziva omega 6-masnom kiselinom, a linoleinska kiselina ima dvostruku vezu između 3. i 4. ugljenikovog atoma i ubraja se u omega 3-masne kiseline. Ljudsko tijelo ne raspolaže enzimom koji razlaže dvostruke veze masnih lanaca većih od 10 ugljikovih atoma. Sve su one u visokom postotku prisutne u sjemenkama i sjemenim uljima. Posljednjih nekoliko godina pažnju fiziologa i farmaceuta zaokuplja gama-linolenska kiselina jer djeluje kao preteča u nastanku tvari koje zovemo prostaglandini-2. To su specijalni hemijski „glasnici“ koje koriste sva tkiva u organizmu. Preko njih može se odrediti biološka dob pojedinog organizma, a neophodni su za sve životne funkcije. Esencijalne masne kiseline se moraju unositi hranom jer se ne mogu sami stvoriti u organizmu. Te su masne kiseline ključne u metabolizmu i presudne su za dobro zdravlje. Sudjeluju u funkcioniranju živčanog tkiva, mrežnice i mozga, dakle ključna je za kognitivnu funkciju mozga, memoriranje, vizualno razlikovanje itd. Omega-3 masne su kiseline ključne za stanične membrane – ako ih nema dovoljno u opskrbi, trpe sve stanice, a time tkiva i organi.
Mikrokonstituenti voća i povrća
Mikrokonstituenti se nalaze u različitim izvorima tj. različitom voću i povrću. Posebno su značajni antioksidanti u voću i povrću kao i ostalim biljnim izvorima.
Pektinske tvari. Pektinske tvari su heterogena grupa prirodnih polimernih spojeva i predstavljaju najrasprostranjenije želirajuće sredstvo. To su poligalakturonidi, a sastojci su »kostura« stanica voća i povrća, osobito jabuka, šljiva i dunja. Osnovna gradivna jedinica je (α) – d – galakturonska kiselina. Uz d – galakturonsku kiselinu u sastavu pektina dolaze i neki drugi spojevi kao što su arabinoza, metilpentoza i dr. Pektinske tvari čine: protopektin prekursor), pektin (pektininska kiselina), pektinat – sol pektininske kiseline, pektinska kiselina i pektati – soli pektinske kiseline.
Pektinske tvari smještene su u središnjoj lameli biljne stanice. Zbog svoje funkcije »biljnog kostura« pektini se funkcijski nalaze u istoj skupini u koioj se nalaze celuloza, hemiceluloza, lignin, gume i guar, a nazivamo ih zajedničkim nazivom biljna vlakna. Zbog funkcije zaštite sluznice pektini spadaju u zaštitna sredstva sluznica. Pektinske kiseline nisu topive u vodi, ali su topive alkalne soli tih kiselina.Neke važnije osobine pektina su:
- pektini se nalaze u voću i povrću kao i gume i imaju osnovnu funkciju održanja konzistencije i
- pektinske otopine u formi gela, kad se dodaju šećer i kiseline, čine bazu u formiranju gela i proizvodnje želiranih proizvoda.
Pektini su slični polisaharidnim gumama, kada su otopljeni u vodi bubre i tvore mrežu u kojoj zadržavaju sve suspendirane čestice. Spadaju u aditive ograničene sa dobrom proizvodnom praksom. Dobivaju se vodenom ekstrakcijom iz jabuka ili citrus plodova. Obilato se koriste u prehrambenoj tehnologiji kao stabilizatori, želirajuća sredstva i ugušćivači marmelada, džemova, voćnih krema, pudinga, itd. (Vidi poglavlje 6.5).
Vitamini. Vitamini se definiraju kao organske zaštitne materije koje se moraju unositi u organizam u malim količinama isto kao što se moraju unositi esencijalne amnokiseline i esencijalne masne kiseline. Fukcija vitamina je esencijalna u enzimskom sistemu metabolizma proteina, ugljikohidrata i masnoća u ljudskom tijelu. Evidentna je njihova uloga u održavanju ljudskog zdravlja.Hemijska priroda vitamina je jako raznovrsna, te i njihove fizičke osobine. Vitamini se konvencionalno dijele u dvije osnovne grupe: topive u vodi (C i neki iz B-kmpleksa) i topive u masnoćama (A, D, E i K). Njihova apsorpcija u ljudskom tijelu zavisi od normalne apsorbcije vitamina u prehrani. Mineralne tvari. Minerali su anorganske tvari. Prirodno se nalaze u tlu i u vodi, a otuda dospiju u biljni organizam. Mnogi minerali su esencijalne tvari, dakle pripadaju tvarima koje ljudski (i životinjski) organizam mora unijeti hranom ili pićem izvana.
Tabela 8. Minerali u voću i povrću
| Minerali | Voće i povrće u kojima se nalaze |
| Kalcij | Tamno zeleno povrće, suho voće |
| Bakar | Zeleno povrće |
| Jod | Luk |
| Željezo | Lisnato povrće, peršun |
| Magnezij | Orasi, lisnato povrće, jabuke, celer, limun, smokve |
| Fosfor | Mahunarke, zeleno povrće, orasi |
| Kalij | Banane, suho voće |
| Selen | Mahunarke, češnjak, paradajz, luk |
| Silicij | Zeleno povrće |
| Sumpor | Kupus, jabuke, mahunarke, luk |
| Cink | Zeleno povrće |
Kiseline. Voće sadrži prirodne kiseline kao što je limunska u naranči i limunu, jabučna u jabuci. Kiseline se nalaze u svim biljnim vrstama, a posebno u kiselim plodovima voća i povrća. To su organske kiseline koje u voću i povrću mogu biti slobodne ili kao sastojci estera. U voću ih ima prosječno 0.1 – 2 % dok u soku može da bude i do 6%. Najvažnije kiseline u voću su: limunska, jabučna, vinska, a manje su zastupljene: octena, jantarna, maslačna i oksalna. U povrću ih je manje do 0.1%. Ove kiseline daju voću kiseo okus i usporavaju djelovanje bakterija. U nekim slučajevima, kao kod povrća, postoji povoljno djelovanje bakterija, kao što je npr. fermentacija kupusa, gdje se uz pomoć bakterija odvija mliječno-kiselinsko vrenje, ili proizvodnja sirćeta iz jabuka. Organske kiseline imaju utjecaja na boju voća i povrća. Stabilnost mnogih pigmenta ovisi o pH vrijednosti a obično imaju neutralan pH indikator. U pogledu kvarenja voća i povrća kiseline imaju značajan doprinos jer smanjuju pH vrijednost. U anaerobnim uvjetima pri pH 4.6 Clostridium botulinum može rasti i proizvoditi letalne toksine. Ova opasnost je odsutna pri pH 4.6 i niže. Sadržaj kiselina i šećera su dva glavna elementa koji imaju utjecaja na okus voća. Odnos šećer/kiselina se veoma često koristi u tehnološkim zahtjevima za voće i nekim vrstama voća i povrća. Mineralne kiseline se nalaze se u voću i povrću u obliku soli: sulfata, fosfata, klorida. Značajno je prisustvo i fenolnih kiselina u vocu i povrcu.
Tabela 9. Fenolne kiseline u vocu i povrću
| Naziv kiseline | Voće i povrće koje sadrži fenolne kiseline | |
| 1 | Elaginska kiselina | Orasi ,jagode , strawberries, kupina, guava, grozdje |
| 2 | Galna | Mango, jagoda , soja |
| 3 | Salicilna | Pepermint, kikiriki |
| 4 | Taninska | Kopriva,čaj, jagodasto voće |
| 5 | Vanilin | Vanila , karanfilić |
| 6 | Capsaicin | Paprika, čili |
| 7 | Curcumin | Kari , slačica |
Biljni pigmenti. Biljni pigmenti daju boju voću i povrću kao i proizvodima koji se od njih proizvode. Najpoznatiji je klorofil u zelenim biljkama, velika skupina karotenoida i flavonoida. Žute i narandžaste boje potječu od karotenoida. To su spojevi koji imaju mnogo nezasićene veza koje lako pucaju . Crvene, plave i ljubičaste boje potječu od flavonoidnih spojeva, posebice antocijana, koji su dobri antioksidansi. Zelena boja potječe od klorofila koji je zaslužan za fotosintezu. Sadržaj pigmenata je relativno nizak ali i u malim koncentracijama daju boju proizvodu. Mogu biti topivi i netopivi u vodi. Često su vezani za druge supstance unutar stanice. Biljni pigmenti se razvijaju tokom zrenja i dozrijevanja.
Taninske tvari. Tanini su složena, polifenolna i bezazotna jedinjenja. Na osnovu gradivnih jedinica i hemijske prirode, mogu se izdvojiti dvije osnovne vrste tanina: hidrolizirajući (pirogalni) i kondenzovani (katehinski) tanini. Mješoviti tanini predstavljaju smješu ove dvije vrste tanina. Pseudo tanini nastaju od gradivnih jedinica tanina, ali imaju manju molekulsku masu. Hidrolizirajući tanini su poliestri galne kiseline (ili njenih derivata) i centralnog molekula šećera (najčešće je to glukoza). Galna kiselina nastaje iz šikiminske kiseline. Kondenzovani tanini stvoreni su kondenzacijaom najčešće dva ili tri molekula flavan3-ola (katehina, epikatekina) ili flavan 3,4-diola (protoantocijanidina ili leukoantacijanidina). Osnovne gradivne jedinice ovih tanina, nastaju metabolizmom acetata. Tanini su vrlo rasprostranjeni u biljnom svijetu a nalaze se u citoplazmi perenhimskih ćelija različitih organa.
Tanini predstavljaju zaštitu od insekata i herbivora. S jedne strane smatra se da su medijatori starenja tkiva jer učestvuju u procesu opadaja lišća, a sa druge postoji mišljenje da su depoi šećera prisutni u mladim voćkama, čijim razlaganjem oslobodjeni šećer doprinosi slasti zrelog voća. Odgovorne su za fenomen posmeđivanja. Tanini u voću oporog okusa i stežu usta, sa svojstvom da uništavaju bjelančevine. Ovaj fenomene uništavanja bjelančevina iskorišten je za štavljenje kože. Osim u voću ima ih i u drugim biljkama i iz kojih se i proizvode (hrastova, cerova, jasenova, orahova i druge kore drveća i voća). Višegodišnje zeljaste biljke sadrže najviše tanina u podzemnim organima. Ima ih više u nezrelom voću. Tokom zrenja razgrađuje ih enzim tanaza. Nepoželjni su u voćnim sokovima, imaju koloidna svojstva. S proteinima, koji u otopini također posjeduju naboj, se talože. Uklanjaju se u procesu bistrenja. Zastupljenost u jagodastom voću je oko 0.02 – 0.037% i u jabučastom oko 0.6%.Tanini iz mušmula, divljih krušaka, jabuka i drugog divljeg voća važni su kao pomoć kod proljeva i za brže zarašćivanje rana, kod ujeda i slično. Za te svrhe koriste se i opore jabuke, orahove ljuske, kora i list, plodovi borovnice, kupine i maline, dunja, oskoruša i razno drugo oporo voće.
Tvari arome. Po hemijskom sastavu to su grupe spojeva: alkoholi, aldehidi, ketoni, karbonske kiseline, esteri, eteri, voskovi, voskovima slične tvari i dr. Lako su isparljive s vodenom parom. Utječu na okus i miris. Aromatičnost ovisi o vrsti i sorti voća odnosno povrća, o koncentraciji spojeva, o dijelu biljke u kojem se nalaze, o molekularnoj težini. Tokom zrenja i dozrijevanja se razvijaju iz prekursora (prethodnika) arome i pojačavaju. Intenzitet arome pojačavaju enzimi. Arome su često po strukturi eterična ulja, isparljivi mirisni sastojci biljaka. Eterična ulja su više ili manje složene smješe različitih isparljivih monoterpena, seskviterpena i fenilpropanskih jedinjenja.
Monotorpeni se javljaju u obliku acikličnih, mono-, bicikličnih, alifatičnih i aromatičnih struktura. Seskviterpeni formiraju još raznovrsnije strukture osnovnog skeleta, zbog dužine lanca C atoma veća je mogućnost različitih ciklizacija. Fenilpropanski sastojci zastupljeni su uglavnom umanjim količinama kao aril ili propenilfenoli i aldehidi. Etarsko ulje, obzirom na njegovu složenost, ne predstavlja nepromjenjiv sistem. Količina ulja i procentualni udio svake komponente zavise od mnogo faktora: genotipa, fenofaze, ontogenetskog razvoja, ekoloških faktora i faktora sredine, načina obrade biljne sirovine, načina izolacije etarskog ulja. Sadržaj etarskog ulja definiše kvalitet aroma.
Kvalitet etarskih ulja je definisan organoleptičkim osobinama:
- fizičkim parametrima (relativna gustina, indeks refrakcije, optička rotacija i rastvorljivost u konsetrovanom etanolu) i
- hemijskim parametrima (kiselinski i estarski broj).
Etarska ulja u biljkama nastaju aktivnošću endogenih i egzogenih sekretornih tkiva koja se mogu javiti u obliku pojedinačnih ćelija u parenhinskim tkivima, žlezdanog epitela šupljina ili kanala ili organizovane i specifične strukture. Na sobnoj temperaturi, etarska ulja su najčešće tečnosti, rijetko imaju viskoznu ili polučvrstu konzistenciju. Lako su pokretljiva, bistra ili slabo obojena, većinom ljutog, aromatičnog ukusa. Već na nižim temperaturama, pojedini sastojci estarskih ulja isparavaju te ulja imaju specifičan miris.
Etarska ulja koriste se u parfimeriji, kozmetičkoj i industriji sredstava za higijenu.U prehrambenoj industriji koriste se kao začini i aditivi. Osiguravaju bolju svarljivost i iskorišćenja hrane. Kao konzervansi produžavaju svježinu hrane a koriste se i u industriji alkoholnih i bezalkoholnih pića.
Enzimi (fermenti). Enzimi su biohemijski katalizatori koji po svom sastavu spadaju u grupu globularnih (klupčastih) proteina koji promoviraju većinu biohemijskih reakcija nastalih u biljnim stanicama. Biomehanizam djelovanja enzima bazira se na specifičnoj hidrolizi određenog supstrata. Postoje dvije osnovne grupe enzima
- autohtoni u stanicama voća i povrća
- mikrobni enzimi (na površini voća i povrća).
U svježem voću i povrću sudjeluju u metaboličkim procesima (rast, zrenje i dozrijevanje). Djeluju za vrijeme prerade i čuvanja (skladištenja). Djelovanje može biti poželjno i nepoželjno. U živom tkivu voća i povrća enzimi kontroliraju reakcije vezane za zrenje i dozrijevanje. Poslije branja voća i povrća, ako nisu inaktivirani zagrijavanjem, kemikalijama ili na drugi način enzimi nastavljaju procese katalize i u mnogim slučajevima izazivaju kvarenje. Zbog toga što učestvuju u mnogim biohemijskim reakcijama u voću i povrću odgovorni su za promjene u aromi i okusu, boji, teksturi i nutritivnim svojstvima. Proces zagrijavanja voća i povrća za vrijeme prerade uzrokuje ne samo uništavanje mikroorganizama nego i deaktivaciju enzima što omogućava produženje upotrebe – konzerviranje. Enzimi imaju optimlnu temperaturu djelovanja oko 40 – 50 °C. Zagrijavanje iznad optimalne temperatue uzrokuje deaktivaciju. Aktivnost svakog enzima je također karakteristika optimalne pH vrijednosti. Specifični su za određenu materiju i djeluju veoma selektivno, npr. proteaza na protein, amilaza na škrob, itd.
Kutikula. Kutikul ili voštanu ovojnicu čine uljne i voštane frakcije koje imaju važnu ulogu u zaštiti plodova od djelovanja atmosferilija, a spriječavaju i transpiraciju , smanjuju respiraciju. Tokom skladištenja povećava se uljna frakcija uz razvoj hlapivih estera.
Sorbit. Sorbit je šesterovalentni alkohol čija količina ovisi o stupnju zrelosti. Nastaje kao međuproizvod pri cijepanju šećera. Nalazi se uglavnom u jabučastom (jabuke, kruške) i koštuničavom (trešnja, šljiva) voću i vrlo malo ili uopće ne u jagodastom i južnom voću.
Glikozidi .Glikozidi se nalaze u manjim količinama u mesu plodova (glukojantarna kiselina). U sjemenkama su prisutni kao amigdalin, limetin, kao i u pokožici (auranciamarin).
Antocijanidini, flavoni i flavonoli dolaze u prirodi u vezanom obliku kao glikozidi. Najčešći glikozidni šećeri su: glukoza, galaktoza, ksiloza, arabinoza i raminoza. Glikozidi antocijanidina zovu se antocijani i crvene su do plave boje, koja je karakteristika brojnih vrsta voća. Flavon i flavonolglikozidi dolaze u svakoj biljnoj vrsti i imaju slabo žutu boju.Vrste glikozida su i saponini, oni sastojci što ih sadrže i šamponi, losioni i slična kozmetička sredstva. Ako dospiju u krvotok iz pripravaka ciklame, a donekle i iz divljeg kestena, izazivaju raspadanje crvenih krvnih tjelešaca. Jako su otrovni za žive tvari stanice, na sluzokoži izazivaju osjećaj draženja i lučenja tekućine, a na osjetljivoj koži mogu kod pojedinaca izazvati saponizidi alergije.
Lignani. Fitoestrogeni – lignani , nazvani tako zbog strukture i učinaka koji su slični estrogenim hormonima. Lignani su veoma rasprostranjeni u biljnom svijetu. Najviše ih ima u lanenim sjemenkama, a nalaze se u jagodičastom voću (secoisolariciresinol), artičokama (silamarin) , sezamu i brokulama (matairesinol).
Alkaloidi. Alkaloidne biljke imaju vrlo velik značaj za čovjeka, za njegov život i rad. Alkaloidi su organske molekule sa nitrogenom, vise poznate zbog svog farmakološkog efekta na ljude i životinje. Nose naziv alkaloidi zbog obavezne komponente nitrogene baze u spoju ( naprimjer amini), pa se mogu smatrati derivatima aminokiselina . Alkaloidi se mogu naći u biljkama ( naprimjer u kromiru i paradjzu) i gljivama. Mogu biti ekstrahirani iz njihovih izvora tretmanom sa kiselinama ( obično HCl i H2SO4 ili maleinskom i limunskom kiselinom ). Većina ih ima gorak okus. Ekstrahuju se iz ljekovitih biljaka, ali su prisutni i u odredjenim vrstama voća i povrća. Proizvode se i sintetski. Alkaloidi se obicno klasificiraju na osnovu zajedničkog molekularnog prekursora, odnosno na bazi biološkog ciklusa putem kojeg se sintetizira molekula. Područje biosinteze alkaloida još nije dovoljno istraženo, pa se alkaloidima daju i nazivi po funkcijama finalnog proizvoda (opijum) ili po biljci odakle je izoliran (solanin). Kad se dovoljno sazna o izvjesnom alkaloidu, klasifikacija se mijenja u svjetlu novih saznanja, a obicno dobija ime biološki vaznih amina koji ucestvuju u procesu sinteze.
Fitohormoni. Fitohormoni (regulatori rasta ) su interni hemijski sekreti u biljkama koji služe kao regulatori njihovog rasta, zrenja i sazrijevanja. Njihove molekule u maloj koncentraciji proizvode signale na specificifičnoj lokaciji, uzrokujući odredjene ciljane procese u stanicama biljke. Postoji pet klasa biljnih hormona :
- auxini
- citokinini
- etilen
- giberelini
- abscisicnska kiselina (ABA)
U ovu grupu spojeva mogu se dodati još :
- brasinosteroidi (BA )
- jasmionati (JA )
- salicilati (SA )
Auxin. Auxin ima funkciju da prevenira izenandnu i neželjenu ekspanziju staničnog volumena.
Auxin naprimjer utiče na rast jagode. Sjeme proizvodi auksin, a kad se ukloni jagoda se ne razvija.
Citokinin promovira konverziju etioplasta u kloroplast stimulacijom klorofilne sinteze u listovima a time i fotosinteze te na taj način usporava starenje listova. Promovira otvaranje stoma na listovima i inducira funkcije ksilema i floeme u biljci. Odgovoran je za porast nivoa minerala i vode.
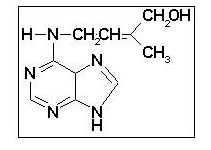
Postpoje dva tipa citokinina : adenin, citokinin i fenil-urea citokinin. Predstavnici adenin-citokinina su: kinetin, zeatin, benzil-adenin. DNA baziran adenin strukturalno je analogan citokininu i ima nižu citokininsku bioaktivnost.
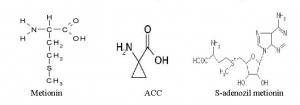
Etilen ( H2C=CH2 ). Etilen ( IUPAC naziv eten) je prosti alken hidrokarbon. Zbog toga što sadrži dvostruku vezu etilen spada u nezasićene ugljikovodonike ili olefine. Još stari egipćani su ga koristili kod stimuliranja sazrijevanja smokvi, a u Kini su ga koristili u zatvorenim sobama za sazrijevanje krušaka. Danas je dobro poznato sredstvo kod skladištenja i čuvanja voća i povrća te značajan biljni hormon. Stimulira dormenciju, zrenje i sazrijevanje voća i povrća. Takodje stimulira otvaranje cvijeta, njegovo starenje (senecenciju) kao i starenje i opadanje lista. Inducira klijanje kod nekih biljnih vrsta.U interferenciji je sa auxinom. Njegova biosinteza započinje od metionina sa 1-aminociklopropan-1-carboksilnom kiselinom (ACC) kao ključnim intermedietom. Esencijalna komponenta u sintezi etilena iz metionina je ATP. Voda i ATP dodane u metionin rezultiraju stvaranjem trifosfata i S-adenozil-metionina (SAM). To podrazumijeva da se ACC se sintetizira iz SAM-a. Oxigen je neophodan da oksidira ACC i prozvede etilen. Ova reakcija katalizirana je sa oksidativnim enzimima koji se zovu etilen formirajući enzimi. U sintezi etilena prvi prekursor je metionin, a simpificirano proces teče sljedećim redom:
Metionin + ATP → SAM → ACC sinteza → ACC → ACC oxidaza → CH2=CH2 + HCN + CO2.
1. ATP reagira sa metioninom pri čemu nastaje SAM
2. SAM je esencialno nosilac forme metionina ( koji je uključen u druge reakcije u stanici )
3. ACC sinteza je krucialna u bioseintezi. Supanj sinteze ACC je limitiran i inducira se:
(a) sazrijevanjem voća;
(b) starenjem cvijeta;
(c) pod djelovanjem IAA ( Indole-3-Acetatne kiseline);
(d) u uvjetima oštećenja plodova;
(e) povredama ploda nastalim promrzavanjem;
(f) netašicom vode- suša;
(g) izloženosti vodi ;
(h) pod djelovanem etilena („jedna loša jabuka pokvari cijlu gomilu“).
4. ACC oxidaza je prethodno nazvana „etilen forming enzim, EFE.“ . Takodje je produkt multigen familije.
5. Jedan od produkata ACC oxidaze je nastanak i aktivnost HCN – što objašnjava zašto većina biljaka posjeduje enzimski sistem za detoxifikaciju ( metabolirajući cijanid) . ACC oxidaza se inhibira pod anaerobnim uvjetima
Metionin se nalazi u voću, povrću i leguminozama i neophodan je u Yangovom ciklusu. Ima ga u spanaću, grašku, mandarinam, kikirikiju, pistacijama, makadamiji itd. S-adenozil metionin (SAM) je enzimski kofaktor uključen transver metil grupe. Nalazi se u svim eukariotskim stanicama. ACC (1-aminociklopropan-1-carboxilnom kiselina) je ciklična aminokiselina. Sintetizira enzimski se iz metionina i konvertira do etilena pomoću ACC oxidaze. ACC sinteza je citosolna i kodirana je multigen familijom.
Giberelinska kiselina. Sintetizira se u embriju proklijalih zrna i u korijenu biljka .Razina u biljci joj poraste u mraku kad se ne obavlja proces fotosinteze .
Abscisinska kiselina ,takodje poznata kao abscisin ( ABA) . Stimulira zatvaranje stoma na listovima. Inhibira zrenje voća. Smanjuje dormenciju sjemena inhibirajući rast stanica i klijanje sjemena. Odgovorna za odbranu od patogena. Inducira starenje u već ostecenim plodovima.
Brasinosteroidi. Ima ih više u zreloj nego u nezreloj stanici. Inhibiraju starenje i opadanje lista, kao i rast korijena.
Jasmonati (JA) su takodje grupa biljnih hormona. Utjecaj im je povezan sa nivoom ABA. Imaju uticaja na sintezu proteina i razinu klorofil u listovima. Inhibiraju rast i klijanje, promoviraju senecenciju , sazrijevanje plodova voća , formiranje pigmenata itd.
Salicilna kiselina .Retardira senescenciju – i vjerovatno inhibira biosintezu etilena. Inducira cvjetanje. Inhibira klijanje , inhibirajući sintezu ABA.
Zaključci
Osnovni hemijski konstituenti voća i povrća su voda i suha tvar. Kvantitativno najznačajniji konstituent je voda koja se na različite načine vezuje u hemijsku kompoziciju voća i povrća. Način vezivanja vode opredjeljuje struktura sadržaja suhe tvari. U sastav suhe tvari ulazi na hiljade spojeva. Možemo ih sve svrstati u makrokonstituente i mikrokonstituente. Makrokonstituenti su ugljični hidrati, lipidi i proteini. Mikrokonstitenti mogu imati različit hemijski sastav kao što je slučaj sa vitaminima, pigmentima i aromatskim tvarima. Veći broj mikrokonstituenata po svojoj prirodi mogu biti ugljični hidrati (pektini, gume, sluziinulin), ali i proteini (enzimi) kao i lipidi ( fosvolipidi). Takodje je i veliki bro složenih hemijskih spojeva konjugiranih lipida, proteina i ugljikohidrata. Na temelju hemijskog sastava odredjuju se prehrambena i druga svojstva voća i povrća.
Citirana i korištena literatura:
1. Grujić R.: „Nauka o ishrani čovjeka“, Tehnološki Fakultet Univerziteta U Banjoj Luci 2000.
2. Karlson P. : „Biohemija“ , Školska knjiga , Zagreb , 1984.
3. Norman N.Potter and Joseph H.Hotchkiss: „Food science“, Chapman&Hall, New York, 5rd edition, 1997
4. HD Belitz, W Grosch: „Food Chemistry“, Springer, Berlin, 3rd edition, 2004
5. TP Coultate: „Food: The chemistry of its components“, Royal Society of Chemistry,Herts, 1995
6. B.S.Luh: »Commercial vegetable processing«, AVI book, New york,1988.
7. James a. Joseph, Daniel A.Nadeau,Anne Anderwood :“Ljekovite boje hrane“,Mozaik knjiga, Zagreb, 2007.
8. Earl Mindell :“Vitaminska biblija za 21 stoljeće“, Mozaik knjiga,zagreb,2001.
9. P.W.Board:“Quality control in fruit and vegetable processing“, FAO, Rome, 1988.
10. Mircea E. D.: „Fruit and vegetable processing“, FAO Agricultural services bulletin No.119, Food and Agriculture Organization of the United Nations, Rome, 1995.
11. L.Samogyi: „Processing fruit -biology, principles and application“, Technomic, Lancaster, 1996.
12. L.Samogyi.: „Processing fruit major processd product“, Technomic, Lancaster,1996.